Aromaten
Aromaten besitzen ein Ringsystem, das wir dir in diesem Beitrag genauer anschauen. Dabei schauen wir uns die Hückel Regel und verschiedene Reaktionsarten an.
Möchtest du das Thema lieber in einem Video kurz erklärt bekommen? Dann schau doch hier mal rein.
Inhaltsübersicht
Aromatische Verbindungen
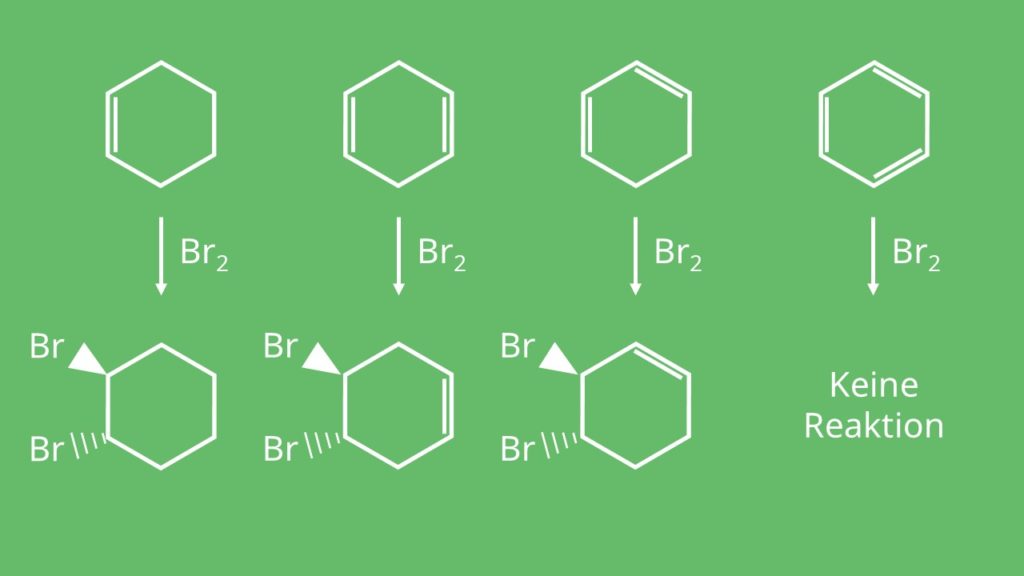
Um das Verhalten von Aromaten genauer zu analysieren, wollen wir dafür verschiedene Cycloalkene bei einer Reaktion mit Brom miteinander vergleichen: Cyclohexen, 1,4-Cyclohexadien, 1,3-Cyclohexen und 1,3,5-Cyclohexatrien oder auch Benzol. Die ersten drei zeigen eine elektrophile Addition wie bei den nicht cyclischen Alkenen. Benzol hingegen ist anders, da es mit Brom keine Reaktion eingeht.
Durch Mesomerie wird Benzol besonders stabilisiert. Mesomerie bedeutet, dass die Bindungsverhältnisse in einem Molekül nicht durch eine einzige Struktur, sondern durch mehrere Grenzformeln dargestellt werden können. Dies geht mit einer erheblichen Stabilisierung einher.
Hückel Regel
Nicht nur Benzol weist diese Eigenschaft auf, sondern alle Moleküle, die die Hückel Regel erfüllen. Diese besagt, dass planare, zyklisch durchkonjugierte Moleküle, die eine ungerade Anzahl an [4n+2] p-Elektronenpaaren haben als Aromaten bezeichnet werden. Zyklisch durchkonjugiert bedeutet einerseits, dass alle C-Atome sp2-hybridisiert sind. Anderseits, dass eine oder mehrere Doppelbindungen durch positiv oder negativ geladene Kohlenstoffatome oder durch andere Atome getrennt sind.
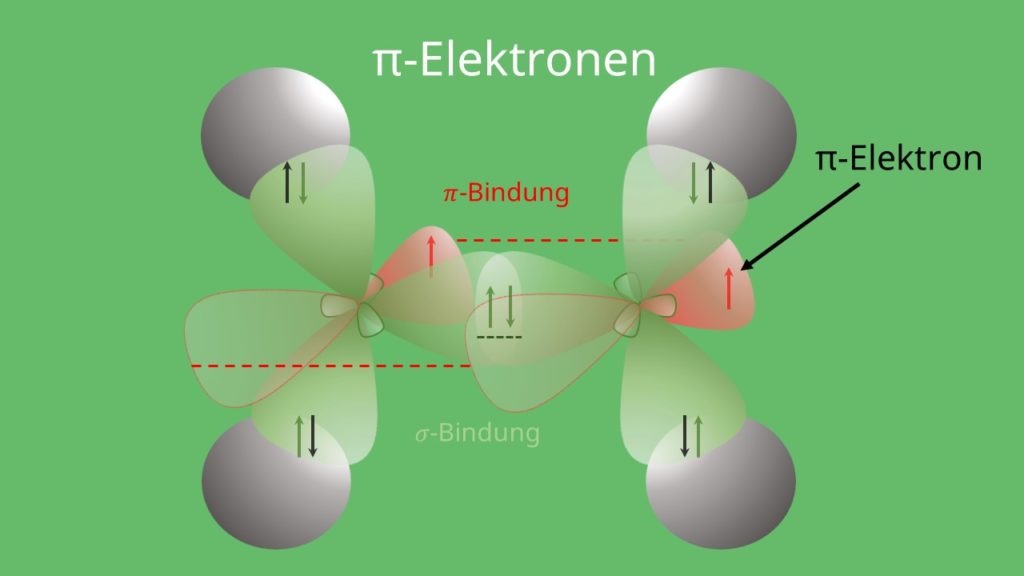
Was die pi-Elektronen angeht, erinnerst du dich vielleicht noch, dass bei einem sp2-hybridisierten Kohlenstoffatom immer vier Elektronen an der Doppelbindung beteiligt sind und ein Elektron in einem reinem pi-Orbital verbleibt. Diese werden hier gezählt.
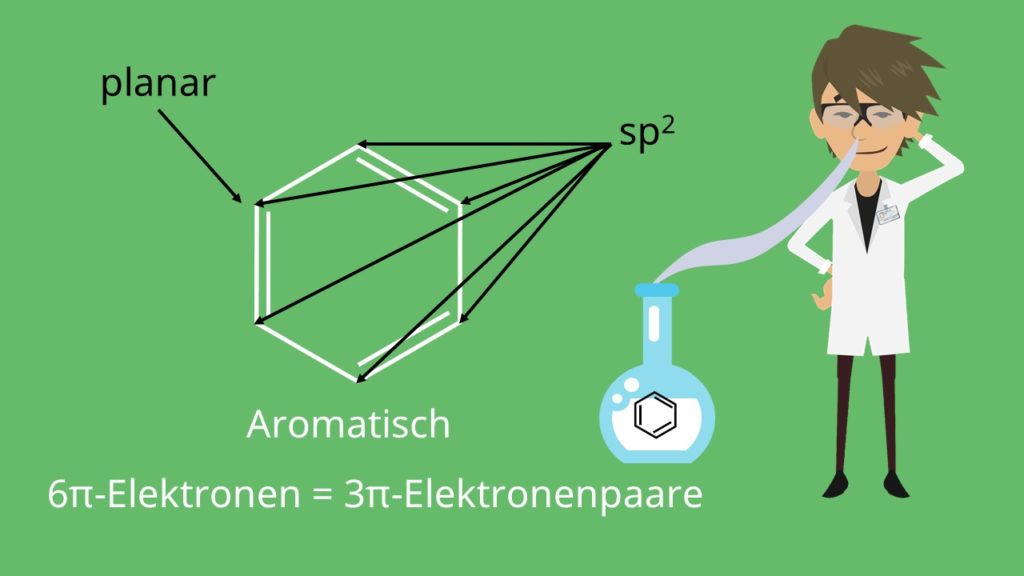
Benzol ist planar und durchgehend sp2-hybridisiert. Wir zählen 6 p-Elektronen, also 3 p-Elektronenpaare, was eine ungerade Anzahl ist. Damit ist die Bedingung für n gleich 1 erfüllt. Benzol ist also aromatisch. Übrigens: Benzol ist eine giftige Flüssigkeit, die einen aromatischen Geruch hat. Daher stammt auch der Name für die Verbindungen dieser Stoffklassen, obwohl die meisten Aromaten kein besonderes Aroma haben. Es wurde früher zum Entkoffeinieren von Kaffee genutzt.
Schauen wir uns ein weiteres Aromat an: Oxazol. Es ist planar und zyklisch durchkonjugiert, da es zwei Doppelbindungen hat, die durch zwei andere Atome abgetrennt sind. Die drei Kohlenstoffatome haben jeweils ein pi-Elektron, kommen zusammen also auf drei. Stickstoff hat drei pi-Elektronen, von dem eins an der Doppelbindung beteiligt ist, und Sauerstoff hat 4: Macht insgesamt 10 pi-Elektronen, also 5 pi-Elektronenpaare. Also eine ungerade Anzahl.
Elektrophile Substitution
So, jetzt weißt du was Aromaten ausmacht. Aber wie können diese jetzt reagieren? Am Anfang hatten wir ja festgestellt, das Brom mit Benzol nicht reagiert, weil Benzol zu stabil ist. Wenn wir aber zu Brom einen Katalysator wie FeBr3 hinzufügen erhalten wir Brombenzol. Dies geschieht allerdings nicht in einer elektrophilen Additionsreaktion, sondern in einer elektrophilen Substitutionsreaktion. Um das zu verstehen, schauen wir uns den Reaktionsmechanismus Schritt für Schritt im Video an.
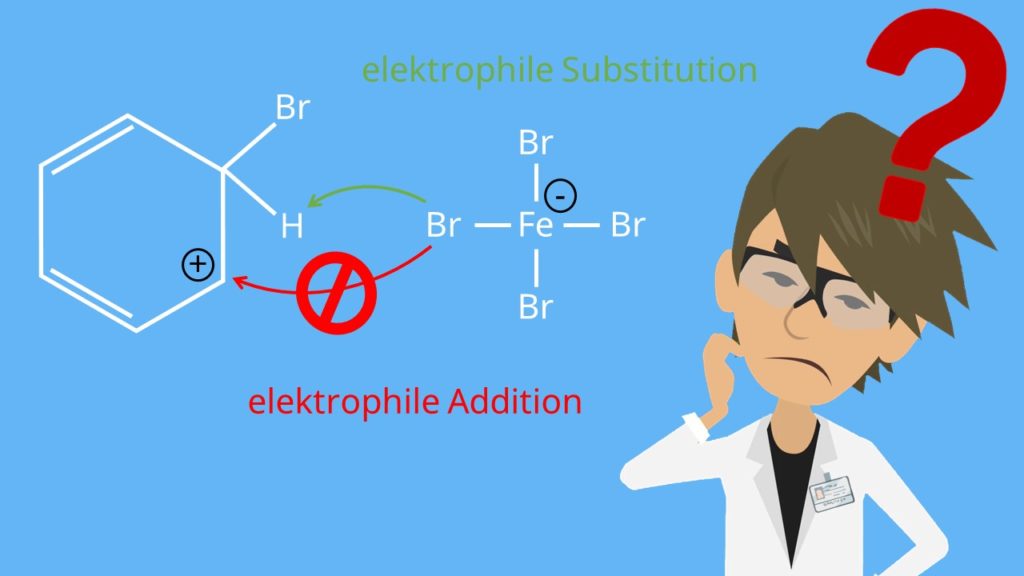
Das Br2 wird polarisiert, sodass das positiv polarisierte Br-Atom wie bei der elektrophilen Addition über beide Kohlenstoffzentren wechselwirkt. Das negativ polarisierte Br-Atom reagiert mit dem FeBr3, wodurch das Fe einen Elektronenüberschuss erfährt. Das Br am Benzol bindet nun an einen Kohlenstoff, wodurch ein anderer Kohlenstoff im Ring positiv geladen sein müsste. Diese positive Ladung ist jedoch durch Mesomerie nicht nur auf eins, sondern auf alle Kohlenstoffatome im Ring verteilt. Diese Stabilisierung führt dazu, dass ein Br am FeBr4–, nicht an ein anderes Kohlenstoffatom im Benzol bindet, wie wir es von der elektrophilen Addition kennen. Es spaltet das Wasserstoffatom am Kohlenstoff, an dem bereits das Br bindet mit der elektrophilen Substitution.
Wir erhalten Brombenzol. Die Addition im zweiten Reaktionsschritt kann mit der elektrophilen Substitution nicht konkurrieren, weil bei der Substitution die Rearomatisierung erreicht wird und diese stabiler ist.
Nietrierung, Sulfonierung und Friedel Craft Alkylierung
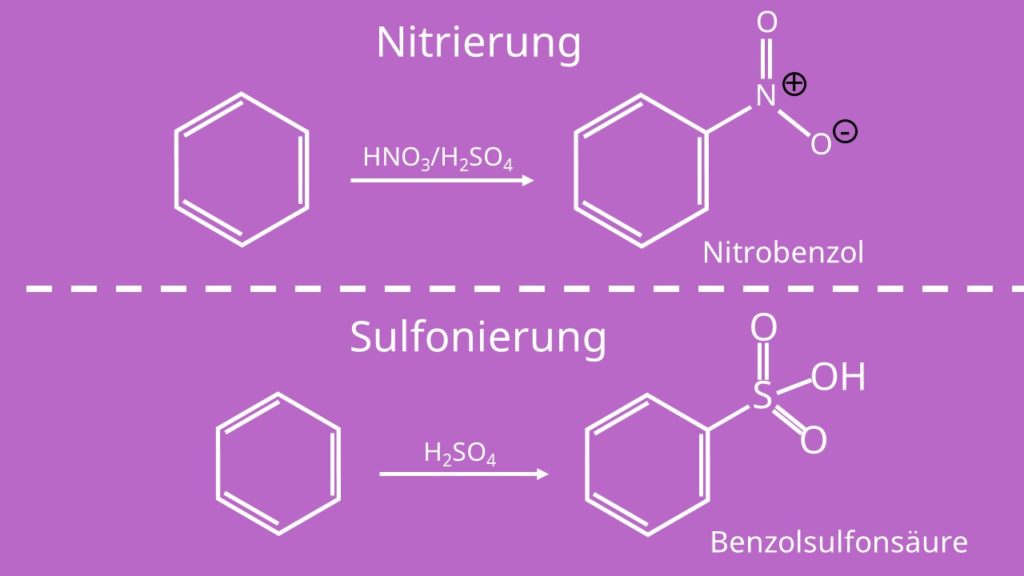
Für die anderen Halogene funktioniert der Schritt analog, nur das man als Katalaysator Fe mit dem jeweiligen Halogen nutzt. Es gibt es noch weitere Reaktionen, die wichtig sind. Diese zeigen wir dir jetzt in Kurzform. Die Nitrierung von Benzol ist eine Reaktion, bei der Benzol mit Salpetersäure und Schwefelsäure als Katalysator umgesetzt wird und Nitrobenzol entsteht.
Bei der Sulfonierung reagiert Benzol nur mit Schwefelsäure und es entsteht Benzolsulfonsäure.
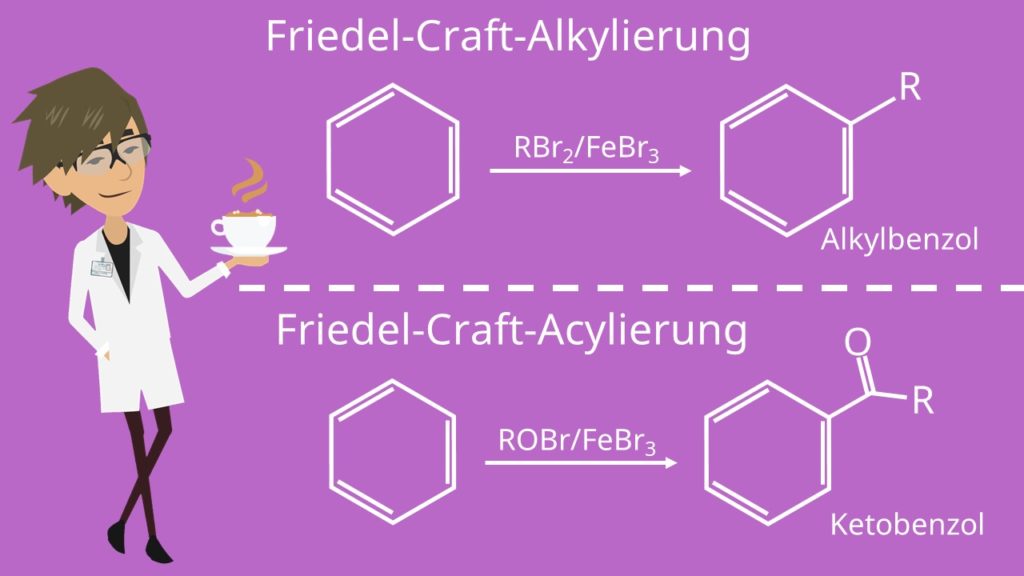
Benannt nach ihren Entdeckern ist die Friedel-Craft-Alkylierung. Hier reagiert Benzol mit einem Alkylbromid und FeBr3 als Katalysator zu einem Alkylbenzol beliebiger Länge.
Du darfst diese Reaktion nicht verwechseln mit der Friedel-Craft-Acylierung. Bei dieser reagiert Benzol mit einem Keton unter FeBr3 zu einem Ketobenzol.