Freie Enthalpie / Gibbs-Energie
Die Gibbs-Energie oder auch Freie Enthalpie ist eine Zustandsgröße, die ein Potential in der Thermodynamik beschreibt. Was es damit auf sich hat, zeigen wir dir in diesem Beitrag.
Inhaltsübersicht
Herleitung der Freien Enthalpie und der Gibbs-Energie
Durch die Ermittlung der Reaktionsenthalpie können wir feststellen, ob eine Reaktion exo- oder endotherm abläuft. Worüber sie uns allerdings keine Auskunft gibt ist, ob die Reaktion freiwillig, also von selbst, abläuft oder eben nicht. Es gibt nämlich auch viele Reaktionen, die zwar spontan beziehungsweise freiwillig ablaufen, bei denen sich das Gemisch aber während der Reaktion abkühlt.
Die Reaktionsfreudigkeit in Form der Gibbs-Energie
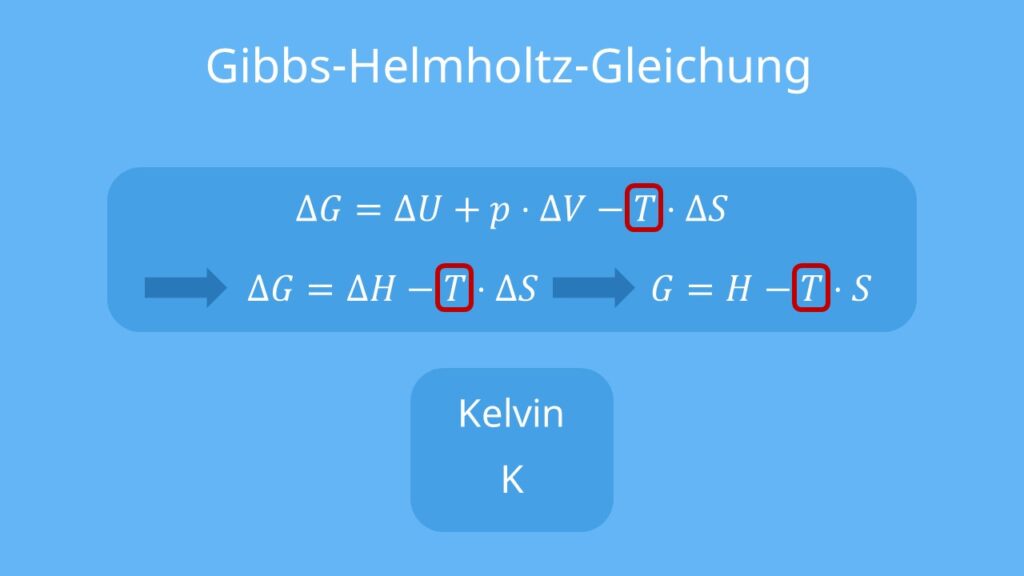
Die sogenannte Triebkraft oder Reaktionsfreudigkeit der Reaktion wird durch die Gibbs-Energie ausgedrückt und als 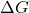 bezeichnet. Sie wird über die Gibbs-Helmholtz-Gleichung mit Hilfe der Enthalpie
bezeichnet. Sie wird über die Gibbs-Helmholtz-Gleichung mit Hilfe der Enthalpie 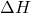 und der Entropie
und der Entropie 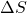 wie folgt ermittelt:
wie folgt ermittelt:

Der Term „ 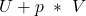 “ beschreibt die Enthalpie und kann damit durch
“ beschreibt die Enthalpie und kann damit durch 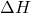 ersetzt werden. Wenn du dir an dieser Stelle nicht mehr ganz sicher bist, wieso das so ist, schau dir doch am besten unser Beitrag zur Enthalpie an.
ersetzt werden. Wenn du dir an dieser Stelle nicht mehr ganz sicher bist, wieso das so ist, schau dir doch am besten unser Beitrag zur Enthalpie an.
Wir erhalten also:
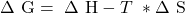
beziehungsweise
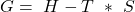
ΔH und ΔS kann man folgendermaßen kombinieren:
| H < 0 | S > 0 | Delta G < 0, immer freiwillig |
T ist für die Intensität bestimmend |
| H < 0 | S < 0 | Temperaturabhängig freiwillig | Dissoziation eines molekularen Gases |
| H > 0 | S > 0 | Freiwillig möglich | Ammoniaksynthese |
| H > 0 | S < 0 | Thermisch nicht möglich | Photosynthese |
Gibbs-Energie
Der Zusammenhang der Temperatur und der Gibbs-Helmholtz- Gleichung
Wie man an der Formel sieht, hängt der Einfluss der Entropie auf die Reaktionsfreudigkeit unmittelbar mit der Temperatur T zusammen. Hierbei solltest du beachten, dass die Temperatur in der Thermodynamik immer als absolute Temperatur in Kelvin angegeben werden muss.
Ähnlich wie bei der Enthalpie gibt es auch bei der freien Enthalpie beziehungsweise Gibbs-Energie weitere intensive Zustandsgrößen. Man unterscheidet auch hier zwischen der molaren und spezifischen Gibbs-Energie.
Die molare Gibbs-Energie wird in Joule pro Mol angegeben und bezieht sich auf die Stoffmenge n.
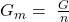
Die spezifische Gibbs-Energie wird in Joule pro kg angegeben und bezieht sich auf die Masse m.
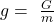
Wie verschiedene Werte der Gibbs-Energie Reaktionen beinflussen
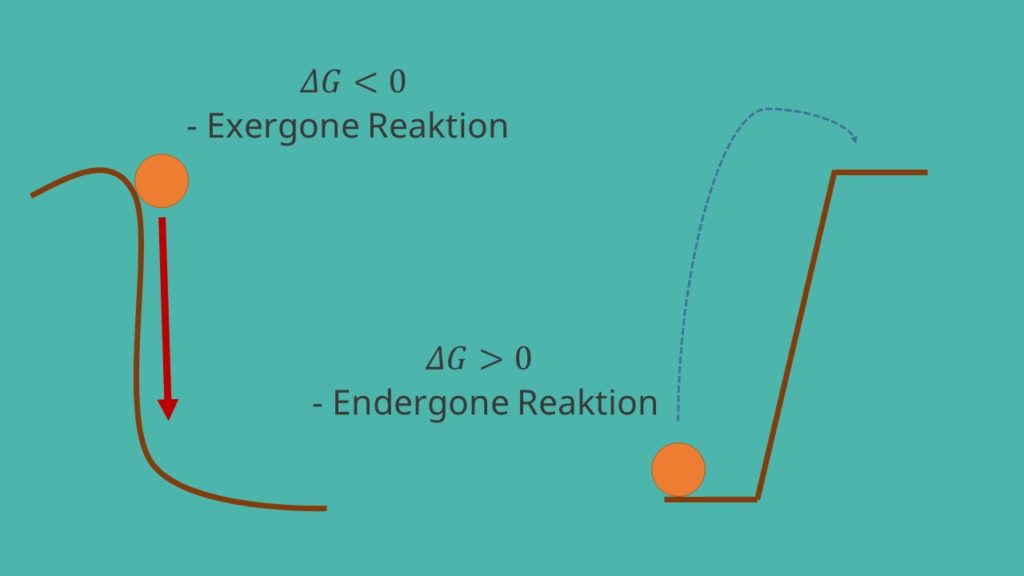
Die Reaktion läuft freiwillig und spontan ab, sobald 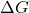 kleiner als 0 ist, es sich also um eine exergone Reaktion handelt.
kleiner als 0 ist, es sich also um eine exergone Reaktion handelt.
Wenn 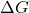 größer als 0 ist, bezeichnet man die Reaktion als endergon. Ist
größer als 0 ist, bezeichnet man die Reaktion als endergon. Ist 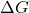 gleich Null, haben wir einen Gleichgewichtszustand vorliegen.
gleich Null, haben wir einen Gleichgewichtszustand vorliegen.
Nun weißt du also wie du beurteilen kannst, ob eine Reaktion von selbst abläuft oder nicht. Viel Erfolg!