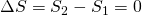Isentrope Zustandsänderung
Was ist eine isentrope Zustandsänderung und wie kannst du sie herleiten? In diesem Artikel erklären wir dir alles, was du über die isentrope Zustandsänderung wissen musst.
Du willst den Inhalt dieses Artikels in unter 5 Minuten verstehen? Dann schau dir gerne unser kurzes und verständliches Video an.
Inhaltsübersicht
Isentrope Zustandsänderung einfach erklärt
Ein isentroper Prozess in der Thermodynamik ist ein Prozess, bei dem sich die Entropie S des Systems nicht verändert.
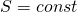
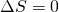
Diese isentropen Prozesse finden in adiabaten reversiblen Systemen statt. Daher erfolgt während der isentropen adiabaten Zustandsänderung kein Wärmeumsatz.
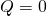
Außerdem ist die Dissipationsarbeit null, weil es sich um einen reversiblen Prozess handelt.
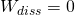
Umgekehrt muss das allerdings nicht zutreffen.
Eine isentrope Zustandsänderung kann auch irreversibel ablaufen, wobei Entropie erst produziert und dann wieder über einen Wärmestrom abgeführt werden muss. In diesem Fall ist der Zustand allerdings nicht mehr adiabat.
Thermische Zustandsgleichungen
Betrachten wir nun die Berechnung der thermischen Zustandsgrößen. Für die Entropieänderung eines idealen Gases gilt:
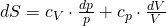
dp und dV beschreiben dabei die Änderung des Druckes und des Volumens. 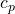 und
und 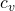 sind die isochore und die isobare spezifische Wärmekapazität des Stoffes.
sind die isochore und die isobare spezifische Wärmekapazität des Stoffes. 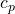 ist dabei stets größer als
ist dabei stets größer als 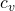 . Isochore Wärmekapazität bedeutet, dass hier die Wärmemenge, die je Kelvin Temperaturerhöhung zugeführt werden muss, bei einem konstanten Volumen angegeben wird. Bei der isobaren Wärmekapazität wird hingegen nur der Druck konstant gehalten.
. Isochore Wärmekapazität bedeutet, dass hier die Wärmemenge, die je Kelvin Temperaturerhöhung zugeführt werden muss, bei einem konstanten Volumen angegeben wird. Bei der isobaren Wärmekapazität wird hingegen nur der Druck konstant gehalten.
Durch Umformen und Einsetzen der Entropieänderung dS=0 ergibt sich:
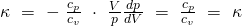
Der Isentropen-Exponent ist grundsätzlich einheitslos und größer als eins. Integrieren und entlogarithmieren wir die Differentialgleichung bei einem konstanten Kappa, dann lautet die Lösung:
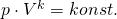
Für zwei beliebige Zustände eines idealen Gases gilt dann:
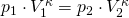
Wenn wir für beide Zustände das ideale Gasgesetz annehmen
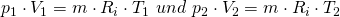
und dieses umformen, dann erhalten wir die thermischen Zustandsgleichungen:
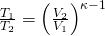
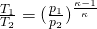
P-V Diagramm
Eine wichtige Darstellungsform ist das p-V-Diagramm. Vergleichen wir den Kurvenverlauf mit dem einer isothermen Zustandsänderung, fällt auf, dass der Verlauf deutlich steiler ist.
Der Grund dafür ist, dass der Exponent des Volumens aufgrund des Isentropenexponentens Kappa größer als eins sein muss.
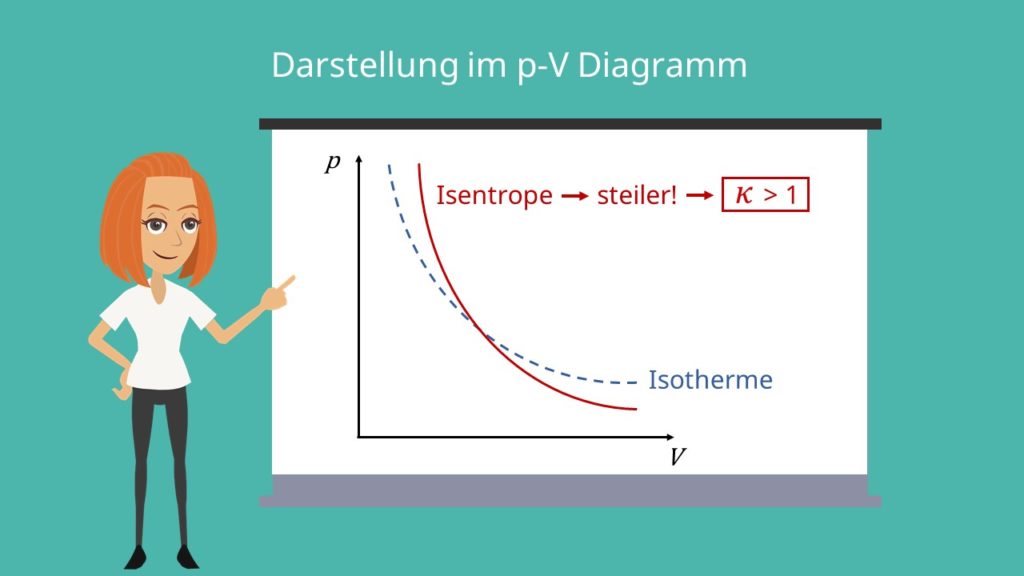
T-S Diagramm
Als nächstes schauen wir uns das T-S Diagramm an. Eine Entropieänderung liegt vor, wenn Wärmeenergie transportiert wird 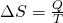 .
.
Da dies beim adiabaten isentropen Prozess nicht der Fall ist, ändert sich die Temperatur nicht und die Isotrope verläuft parallel zur y-Achse.
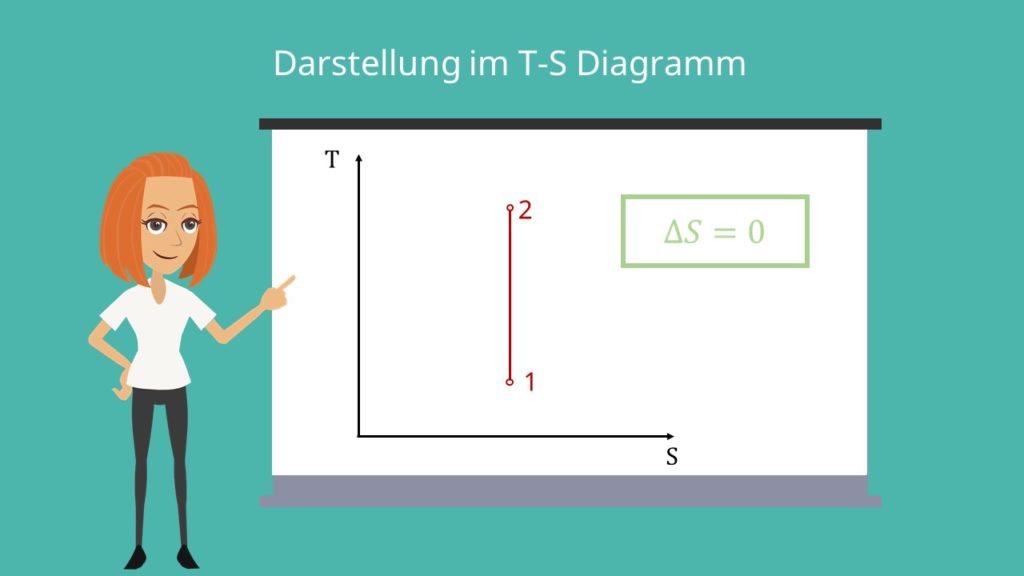
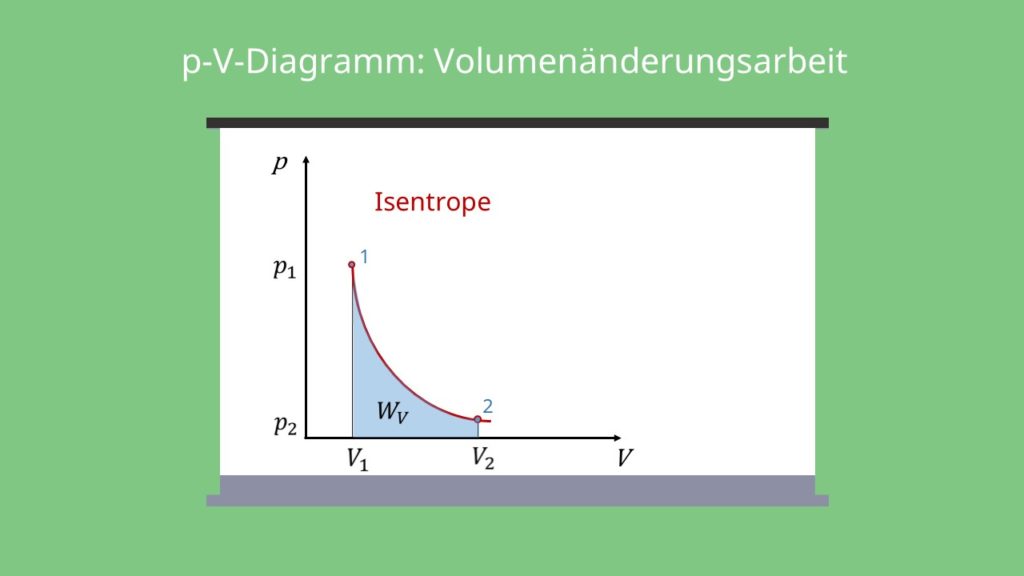
Volumenänderungsarbeit
Die Volumenänderungsarbeit ist die Fläche unter der Isentropen im p-V-Diagramm.
Sie kann mit der Formel für die inneren Energie berechnet werden. Dabei ergeben sich sechs mögliche Methoden, um die Volumenänderungsarbeit zu berechnen. Wir werden hier die drei wichtigsten besprechen. Es gilt:
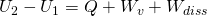
Da wir hier von einem adiabaten System ausgehen, kann die Formel gekürzt werden:
(1) 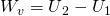
Dies ist unsere erste Gleichung. Eine weitere Möglichkeit ist die Verwendung der kalorischen Gleichung der Volumenänderungsarbeit in Verbindung mit den thermischen Zustandsgleichungen für ideale Gase.
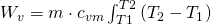
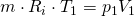
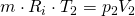
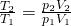
Durch umformen und einsetzen dieser Gleichungen erhalten wir die zweite und dritte Gleichung für die Volumenänderungsarbeit:
(2) 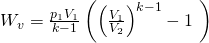
(3) 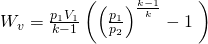
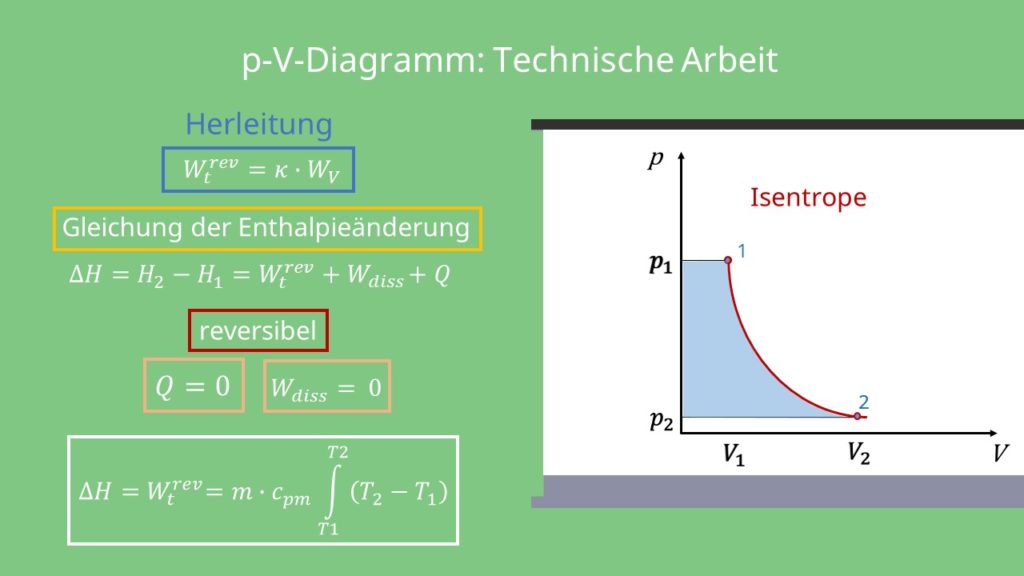
Reversible technische Arbeit
Die technische Arbeit, auch Druckänderungsarbeit genannt, ist die Fläche neben der Isentropen bis zur Druck-Achse im p-V-Diagramm.
Wir können diese berechnen, indem wir die Volumenänderungsarbeit mit dem Isentropenexponenten multiplizieren:
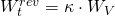
Mathematisch kann diese Formel wie folgt aus der Gleichung aus der Änderung der Enthalpie abgeleitet werden.
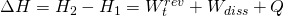
Da hier ein reversibler Prozess vorliegt, sind 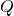 und
und 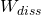 gleich null. Deshalb kannst du die Enthalpieänderung auch so schreiben:
gleich null. Deshalb kannst du die Enthalpieänderung auch so schreiben:
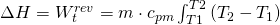
Beachten wir den folgenden Zusammenhang von Kappa, formen diesen nach c p m um und setzten ihn in die Formel für die Enthalpieänderung ein
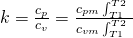
Erhalten wir für die technische Arbeit folgenden Ausdruck:
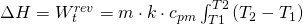
Wie wir bereit wissen ist 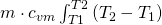 die Volumenänderungsarbeit. Fasst man dies wiederum zusammen, ergibt sich unsere anfängliche Formel der technischen Arbeit
die Volumenänderungsarbeit. Fasst man dies wiederum zusammen, ergibt sich unsere anfängliche Formel der technischen Arbeit
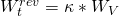
Sehr schön! Nun kannst du die thermischen Zustandsgleichungen aufstellen und die Volumenarbeit berechnen. Außerdem kennst du die reversible technische Arbeit.
Ergänzung zu Volumenänderungsarbeit
Die Volumenänderungsarbeit ist die Fläche unter der Isentropen im p-V-Diagramm .
Sie kann mit der Formel für die inneren Energie berechnet werden. Dabei ergeben sich sechs mögliche Methoden, um die Volumenänderungsarbeit zu berechnen.
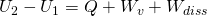
Da wir hier von einem adiabaten System ausgehen, kann die Formel gekürzt werden:
(1) 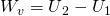
Eine weitere Möglichkeit ist die Verwendung der kalorischen Gleichung:
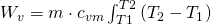
Wir formen die folgende Gleichung nach 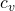 um und setzen sie oben ein:
um und setzen sie oben ein:
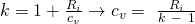
Damit erhalten wir die zweite Methode.
(2) 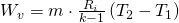
Nun kann die Klammer aufgelöst werden und die thermische Zustandsgleichung idealer Gase in die Formel eingesetzt werden.
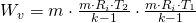
Mit 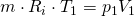
Mit 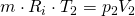
Wir erhalten die dritte Gleichung:
(3) 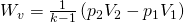
Für die vierte Methode nehmen wir wiederum die thermischen Zustandsgleichungen idealer Gase und teilen sie durcheinander.
Mit 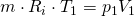
Mit 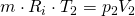
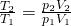
Wir formen nach 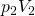 um und setzten sie in die dritte Gleichung ein.
um und setzten sie in die dritte Gleichung ein.
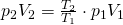
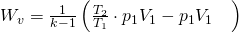
Durch ausklammern von 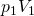 ergibt sich die vierte Gleichung für die Volumenänderungsarbeit:
ergibt sich die vierte Gleichung für die Volumenänderungsarbeit:
(4) 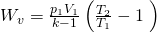
Die fünfte und sechste Gleichung leitet sich ebenfalls aus den bereits dargestellten Zusammenhängen ab und sehen so aus:
(5) 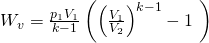
(6) 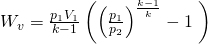
Welche der Gleichungen angewendet wird, hängt von den gegebenen Größen ab.
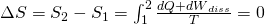
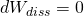 null ist, gilt:
null ist, gilt: