Seiliger Prozess
Der Seiliger Prozess ist eine Mischung aus Otto und Diesel Prozess . Warum wir diese Aussage tätigen können, erfährst du hier.
Inhaltsübersicht
Seiliger Prozess – Gleichraum- und Gleichdruckprozess
In der Realität verläuft die Verbrennung weder beim Otto Prozess komplett isochor noch beim Diesel Prozess komplett isobar . Es handelt sich eher um eine Kombination aus beiden. Dies schlug auch Myron Seiliger in seinem Seiliger Prozess vor, in welchem die Verbrennung durch eine isochore und isobare Wärmezufuhr angenähert wird. Wir können auch von einem Gleichraum- und Gleichdruckprozess sprechen.
Die Untersuchung des Seiliger Prozesses findet unter der Annahme statt, dass wir uns in einem geschlossenen System mit idealem Gas als Arbeitsfluid befinden. Um die Prozesse durchzugehen, betrachten wir das p-V- sowie das T-s-Diagramm . Im Wesentlichen unterscheidet sich der Verlauf nicht großartig vom Otto und Diesel Prozess. Fangen wir an!
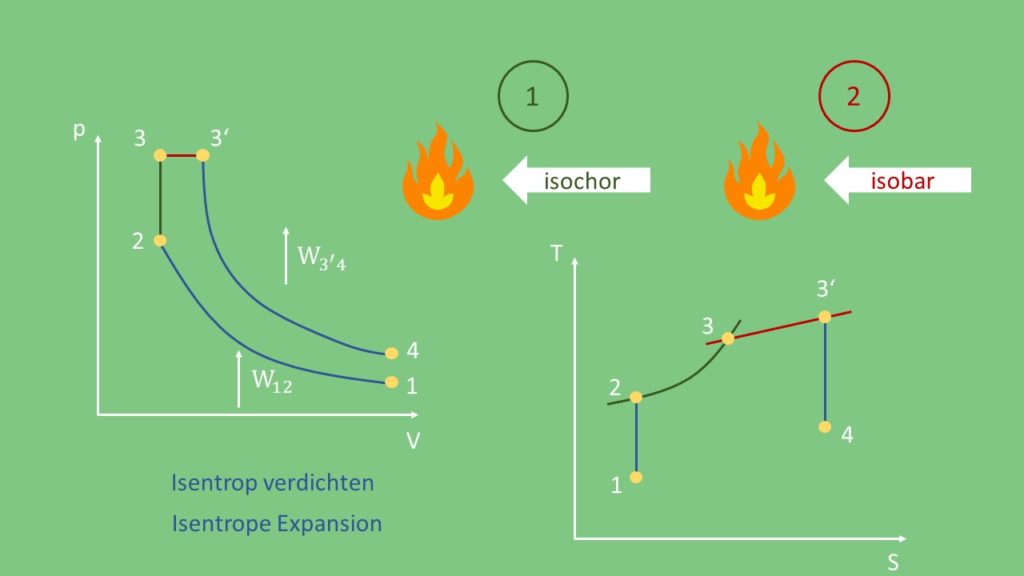
Seiliger Prozess im p-V- und T-S-Diagramm
Zunächst rufen wir uns noch einmal die 4 Takte eines Verbrennungsmotors ins Gedächtnis: Ansaugen, Verdichten, Expandieren und Ausstoßen.
Die Prozesschritte bzw. Takte beim Seiliger Prozess unterscheiden sich vom Otto und Diesel Prozess durch die Aufteilung der Verbrennung in zwei separate Vorgänge. Die Prozessschritte sind:
- Isentrope Kompression
- Isochore Kompression und Wärmezufuhr
- Isobare Expansion und Wärmezufuhr
- Isentrope Expansion
- Isochorer Ladungswechsel
Isentrope Kompression 1 -> 2:
In unserem Vergleichsprozess wird das Gas als erstes isentrop verdichtet. Dazu wird Arbeit 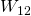 zugeführt.
zugeführt.
Der Druck im System steigt, während das Volumen sinkt. Da die Zustandsänderung ohne Wärmeaustausch mit der Umgebung stattfindet, bleibt die Entropie konstant und die Temperatur steigt.
Isochore Kompression und Wärmezufuhr 2 -> 3:
Nun folgt der Unterschied zum Otto- und Diesel Prozess. Die Verbrennung bzw. Wärmezufuhr teilt sich in zwei Vorgänge auf. Im ersten Schritt wird dem System isochor Wärme zugeführt. Das Volumen bleibt konstant und der Druck steigt.
Isobare Expansion und Wärmezufuhr 3 -> 3′:
Im zweiten Schritt wird dem System isobar Wärme zugeführt. Dabei bleibt der Druck konstant und das Volumen steigt.
Im T-s-Diagramm bedeutet das für beide Verbrennungsvorgänge, dass die Temperatur und die Entropie aufgrund der Wärmezufuhr erhöht werden.
Isentrope Expansion 3‘ -> 4:
Es folgt eine isentrope Expansion des Gases, bei der Arbeit 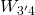 abgegeben wird. Aufgrund der Vergrößerung des Volumens sinkt hier der Druck. Die Entropie bleibt wieder konstant und die Temperatur sinkt.
abgegeben wird. Aufgrund der Vergrößerung des Volumens sinkt hier der Druck. Die Entropie bleibt wieder konstant und die Temperatur sinkt.
Isochorer Ladungswechsel 4 -> 1:
Der letzte Schritt ist der isochore Ladungswechsel, bei dem die heißen Abgase ausgestoßen werden und kühle, frische Luft angesaugt wird. In Folge dessen sinken die Temperatur und die Entropie. Im p-V-Diagramm bleibt das Volumen konstant und der Druck sinkt.
Weitere Vergleichsprozesse
Berechnung des Seiliger Prozesses
Um den Seiliger Prozess mit anderen Verbrennungsprozessen vergleichen zu können, müssen wir wissen, wie wir diesen berechnen können. Neben dem Verdichtungsverhältnis Epsilon 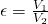 und dem Einspritzverhältnis Phi
und dem Einspritzverhältnis Phi 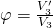 kommt hier noch das Druckverhältnis
kommt hier noch das Druckverhältnis 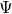 hinzu:
hinzu:
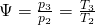
Die Nutzarbeit können wir nun wieder aus der Wärmebilanz ermitteln. Es gilt:
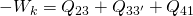
Liegen uns die thermodynamischen Parameter vor, dann erhalten wir:
![Rendered by QuickLaTeX.com -W_k = c_v \cdot [T_1 - T_2 + (1 - \kappa) \cdot T_3 + \kappa \cdot T_{3'} - T_4}]](https://d1g9li960vagp7.cloudfront.net/wp-content/ql-cache/quicklatex.com-82a1d4d8eba3ce91e536d2ba3834ff7b_l3.png)
Kappa 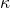 ist der Isentropenexponent und
ist der Isentropenexponent und 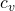 die isochore spezifische Wärmekapazität, die wir mit Hilfe der universellen Gaskonstante und dem Isentropenexponenten darstellen können (
die isochore spezifische Wärmekapazität, die wir mit Hilfe der universellen Gaskonstante und dem Isentropenexponenten darstellen können (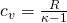 ).
).
Wir können nun zunächst die Temperaturen der einzelnen Zustände in Abhängigkeit von T1 und mit den vorhin genannten Verhältnissen (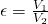 ;
; 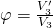 ;
; 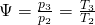 ) ausdrücken.
) ausdrücken.
Diese können wir dann in die Formel für die Nutzarbeit einsetzen und erhalten:
![Rendered by QuickLaTeX.com -W_k = \frac {R \cdot T_1}{\kappa -1} \cdot \{ 1 + \epsilon^{ \kappa - 1} \cdot [ \Psi \cdot (1 - \kappa \cdot (1 - \varphi) ) - 1 ] - \Psi \cdot \varphi^{ \kappa} \}](https://d1g9li960vagp7.cloudfront.net/wp-content/ql-cache/quicklatex.com-350a497c7c9454e25d1c87a99e10f031_l3.png)
Sie ist damit neben der Temperatur abhängig von der universellen Gaskonstanten R, dem Isentropenexponenten 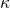 , dem Verdichtungsverhältnis
, dem Verdichtungsverhältnis  , dem Einspritzverhältnis
, dem Einspritzverhältnis 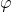 und dem Druckverhältnis
und dem Druckverhältnis 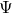 .
.
Wirkungsgrad des Seiliger Prozesses
Schauen wir uns nun an wie wir den thermischen Wirkungsgrad berechnen können. Dieser ergibt sich wieder aus zu- und abgeführter Arbeit. Wir halten fest:
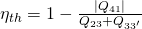
Verwenden wir wieder unsere Verhältnisparameter, dann erhalten wir:
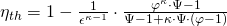
Der Wirkungsgrad steigt bei Erhöhung des Verdichtungsverhältnisses Epsilon, mit sinkendem Einspritzverhältnis Phi und steigendem Druckverhältnis Psi. Mit Hilfe dieser Formel können wir den Wirkungsgrad mit dem von anderen Verbrennungsmotoren sehr gut vergleichen.
Fassen wir nochmal kurz zusammen was wir gelernt haben. Der Seiliger Prozess ist eine Mischung des Otto und Diesel Prozesses. Er enthält zwei isentrope, zwei isochore und eine isobare Zustandsänderung. Die Verbrennung verläuft in zwei Teilen. Einmal isochor und einmal isobar.