Ein chemisches Element kann nicht mehr in andere Stoffe zerlegt werden. Aber was ist ein chemisches Element genau und wie viele chemische Elemente gibt es? Das erfährst du in diesem Beitrag und im Video !
Inhaltsübersicht
Was ist ein chemisches Element?
Ein chemisches Element (oft auch abgekürzt als: chem. Element oder chem Element) ist ein Reinstoff, den du nicht mehr durch chemische Verfahren in andere Stoffe zerlegen kannst. Deshalb sind chemische Elemente auch die Grundbausteine von chemischen Reaktionen. Die kleinste mögliche Menge eines chemischen Elements ist ein Atom.
Du kannst dir hier merken, dass alle Atome eines Elements immer die gleiche Kernladungszahl (Ordnungszahl) besitzen. Das bedeutet, dass sie die gleiche Anzahl an Protonen (positiv geladene, subatomare Teilchen) im Atomkern enthalten. Der Aufbau der Elektronenhülle ist dann ebenfalls gleich, weswegen sich alle Atome eines Elements chemisch identisch verhalten.
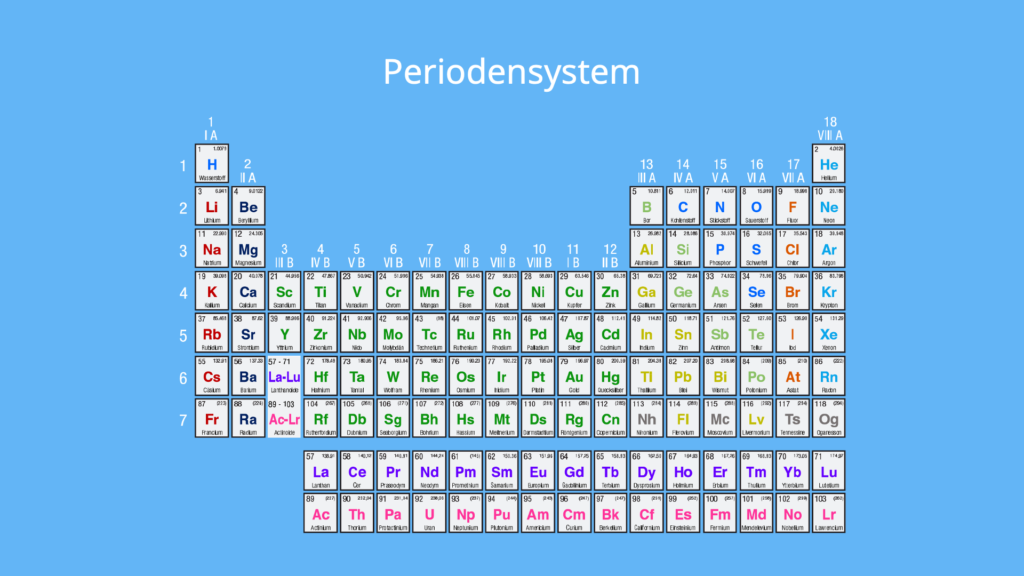
Die Elemente in der Chemie kommen unterschiedlich häufig vor und können auch chemische Verbindungen eingehen. Um die chemischen Elemente sinnvoll zu ordnen, gibt es das Periodensystem. Dort sind die Namen der einzelnen Elemente abgekürzt. Sie tauchen also als chemisches Symbol (Elementsymbol), das maximal aus zwei Buchstaben besteht, auf.
Bis heute konnten 118 chemische Elemente nachgewiesen werden. Alle chemischen Elemente zeigen wir weiter unten in einer Tabelle aufgelistet.
Ein chemisches Element (engl. chemical element) ist ein Reinstoff, der nur aus Atomen gleicher Kernladungszahl besteht. Die einzelnen Elemente unterscheiden sich deshalb durch die Anzahl der Protonen im Atomkern.
Geschichte der chemischen Elemente
Bevor der Begriff chemisches Element, wie wir ihn heute kennen, existiert hat, hatte er noch eine andere Bedeutung: Früher haben die Menschen ein Element noch nach der Vier-Elementen-Lehre definiert. Das heißt, sie waren der Meinung, es gibt nur vier Elemente: Feuer, Wasser, Erde und Luft.
Der Naturforscher Robert Boyle war einer der ersten Wissenschaftler, der die Lehre angezweifelt hat. Er war der Meinung, dass gemischte Stoffe aus chemischen Elementen bestehen. Das heißt, man kann die gemischten Stoffe in ihre einzelnen chemischen Elemente zerlegen.
Der Chemiker Antoine de Lavoisier hat die Theorie weiter entwickelt. Er kam zu dem Schluss, dass chemische Elemente durch keine chemischen Verfahren zerlegt werden können und auch nicht ineinander überführbar sind.
Die Idee, für jedes Element ein chemisches Zeichen einzuführen, stammt von dem Chemiker Jöns Jacob Berzelius. Seine Idee hat sich durchgesetzt, denn bis heute werden chemische Symbole für die Elemente verwendet.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Chemische Elemente Ordnungssystem
Die chemischen Elemente sind also alle im Periodensystem geordnet zu finden. Sie sind aber nicht irgendwie angeordnet, sondern nach steigender Kernladungszahl (Ordnungszahl). Elemente sind im Periodensystem in Gruppen (Spalten) und Perioden (Reihen) aufgeführt.
Auf die Weise kannst du oft schnell bestimmte Eigenschaften wie die Elektronegativität eines Elements herausfinden. Das liegt daran, dass Elemente derselben Gruppe bzw. Periode oft die gleichen Eigenschaften besitzen. Zum Beispiel haben alle Elemente der zweiten Periode eine größere Elektronegativität als die Elemente in der sechsten Periode.
Grob unterscheidest du bei den Elementen zwischen Metall und Nichtmetall.
Chemische Verbindungen
Die meisten Elemente in der Chemie können chemische Verbindungen (kurz: chem. Verbindungen) eingehen. Dabei sind dann die einzelnen Atome zu Molekülen oder Ionenkristallen zusammengeschlossen.
Es verbinden sich nicht immer unterschiedliche Elemente / Atome miteinander, sondern es können sich auch dieselben Elemente miteinander verbinden. Elemente, die meistens als zweiatomige Moleküle auftreten, hast du in der Schule wahrscheinlich mit der Eselsbrücke HOFBrINCl kennengelernt. Dabei geht es um die Elemente Wasserstoff (H), Sauerstoff (O), Fluor (F), Brom (Br), Iod (I), Stickstoff (N) und Chlor (Cl). Sie kommen dann als H2, O2, F2 usw. vor. Bei Wasserstoff, Sauerstoff, Fluor und Stickstoff handelt es sich übrigens um gasförmige chemische Elemente.
Bei einer chem. Verbindung zwischen verschiedenen Elementen unterscheidest du drei Arten:
- Molekulare Verbindungen: Entstehen aus zwei oder mehreren Nichtmetallen. Beispiele: Wasser (H2O), Methan (CH4)
- Ionische Verbindungen: Entstehen aus Metall und Nichtmetall. Dabei müssen die beiden eine unterschiedliche Ladung besitzen. Das heißt, das Metall muss z.B. positiv geladen sein (Kation ) und das Nichtmetall ist dann negativ geladen (Anion ). Beispiele: Natriumchlorid = Kochsalz (aus Na+ und Cl–), Eisen(II)-oxid (aus Fe2+ und O2-)
- Metallische Verbindungen: Entstehen aus zwei oder mehr Metallen. Beispiele: Titanaluminid (Ti3Al), Magnesiumsilicid (Mg2Si)
Reinelemente und Mischelemente
Manche chemischen Elemente weisen in ihrem natürlichen Vorkommen nur eine Sorte von Atomen auf. Sie nennst du dann Reinelemente. Sobald aber ein chemisches Element aus zwei oder mehr Atomsorten (Isotopen) besteht, nennst du es ein Mischelement. Bei Isotopen ist die Anzahl an Protonen im Atomkern gleich. Sie unterscheiden sich nur durch ihre Neutronenzahl.
Es existieren 19 stabile Reinelemente, der Rest sind Mischelemente. Da es 118 Elemente gibt, kannst du sagen, dass die meisten davon Mischelemente sind. Du weißt nicht mehr genau was ein Isotop ist und hättest gerne Beispiele zu Isotopen? Dann schau dir unser Video dazu an!
Chemische Elemente Tabelle
Bisher wurden 118 Elemente in der Chemie nachgewiesen. Wir haben hier alle Elemente für dich aufgelistet:
| LEGENDE | |||||
| Alkalimetalle | Lanthanoide | Übergangsmetalle | Halbmetalle | Halogene | |
| Metalle | Actionoide | Erdalkalimetalle | Nichtmetalle | Edelgase | |
| unbekannt |
| Ordnungszahl (OZ) | Chemisches Symbol | Elementname (nach IUPAC) | Element-kategorie | Atomare Masse (in u) |
| 1 | H | Wasserstoff (Hydrogenium) | Nichtmetall | 1,01 |
| 2 | He | Helium | Edelgas | 4 |
| 3 | Li | Lithium | Alkalimetall | 6,94 |
| 4 | Be | Beryllium | Erdalkalimetall | 9,01 |
| 5 | B | Bor | Halbmetall | 10,81 |
| 6 | C | Kohlenstoff (Carbonium) | Nichtmetall | 12,01 |
| 7 | N | Stickstoff (Nitrogenium) | Nichtmetall | 14,01 |
| 8 | O | Sauerstoff (Oxygenium) | Nichtmetall | 16 |
| 9 | F | Fluor | Halogen | 19 |
| 10 | Ne | Neon | Edelgas | 20,18 |
| 11 | Na | Natrium | Alkalimetall | 22,99 |
| 12 | Mg | Magnesium | Erdalkalimetall | 24,3 |
| 13 | Al | Aluminium | Metall | 26,98 |
| 14 | Si | Silicium | Halbmetall | 28,09 |
| 15 | P | Phosphor | Nichtmetall | 30,97 |
| 16 | S | Schwefel | Nichtmetall | 32,07 |
| 17 | Cl | Chlor | Halogen | 35,45 |
| 18 | Ar | Argon | Edelgas | 39,94 |
| 19 | K | Kalium | Alkalimetall | 39,1 |
| 20 | Ca | Calcium | Erdalkalimetall | 40,08 |
| 21 | Sc | Scandium | Übergangsmetall | 44,96 |
| 22 | Ti | Titan | Übergangsmetall | 47,88 |
| 23 | V | Vanadium | Übergangsmetall | 50,94 |
| 24 | Cr | Chrom | Übergangsmetall | 52 |
| 25 | Mn | Mangan | Übergangsmetall | 54,9 |
| 26 | Fe | Eisen (Ferrum) | Übergangsmetall | 55,85 |
| 27 | Co | Cobalt | Übergangsmetall | 58,93 |
| 28 | Ni | Nickel | Übergangsmetall | 58,69 |
| 29 | Cu | Kupfer (Cuprum) | Übergangsmetall | 63,55 |
| 30 | Zn | Zink | Übergangsmetall | 65,39 |
| 31 | Ga | Gallium | Metall | 69,72 |
| 32 | Ge | Germanium | Halbmetall | 72,61 |
| 33 | As | Arsen | Halbmetall | 74,92 |
| 34 | Se | Selen | Halbmetall | 78,96 |
| 35 | Br | Brom | Halogen | 79,9 |
| 36 | Kr | Krypton | Edelgas | 83,8 |
| 37 | Rb | Rubidium | Alkalimetall | 85,45 |
| 38 | Sr | Strontium | Erdalkalimetall | 87,62 |
| 39 | Y | Yttrium | Übergangsmetall | 88,91 |
| 40 | Zr | Zirconium | Übergangsmetall | 91,22 |
| 41 | Nb | Niob | Übergangsmetall | 92,91 |
| 42 | Mo | Molybdän | Übergangsmetall | 95,94 |
| 43 | Tc | Technetium | Übergangsmetall | 98,91 |
| 44 | Ru | Ruthenium | Übergangsmetall | 101,07 |
| 45 | Rh | Rhodium | Übergangsmetall | 102,91 |
| 46 | Pd | Palladium | Übergangsmetall | 106,42 |
| 47 | Ag | Silber | Übergangsmetall | 107,87 |
| 48 | Cd | Cadmium | Übergangsmetall | 112,41 |
| 49 | In | Indium | Metall | 114,82 |
| 50 | Sn | Zinn (Stannum) | Metall | 118,71 |
| 51 | Sb | Antimon (Stibium) | Halbmetall | 121,75 |
| 52 | Te | Tellur | Halbmetall | 127,6 |
| 53 | I | Iod | Halogen | 126,9 |
| 54 | Xe | Xenon | Edelgas | 131,29 |
| 55 | Cs | Caesium | Alkalimetall | 132,91 |
| 56 | Ba | Barium | Erdalkalimetall | 137,33 |
| 57 | La | Lanthan | Übergangsmetall | 138,9 |
| 58 | Ce | Cer | Lanthanoid | 140,11 |
| 59 | Pr | Praseodym | Lanthanoid | 140,91 |
| 60 | Nd | Neodym | Lanthanoid | 144,24 |
| 61 | Pm | Promethium | Lanthanoid | 146,92 |
| 62 | Sm | Samarium | Lanthanoid | 150,36 |
| 63 | Eu | Europium | Lanthanoid | 151,96 |
| 64 | Gd | Gadolinium | Lanthanoid | 157,25 |
| 65 | Tb | Terbium | Lanthanoid | 158,93 |
| 66 | Dy | Dysprosium | Lanthanoid | 162,5 |
| 67 | Ho | Holmium | Lanthanoid | 164,93 |
| 68 | Er | Erbium | Lanthanoid | 167,26 |
| 69 | Tm | Thulium | Lanthanoid | 168,93 |
| 70 | Yb | Ytterbium | Lanthanoid | 173,04 |
| 71 | Lu | Lutetium | Lanthanoid | 174,97 |
| 72 | Hf | Hafnium | Übergangsmetall | 178,49 |
| 73 | Ta | Tantal | Übergangsmetall | 180,95 |
| 74 | W | Wolfram | Übergangsmetall | 183,85 |
| 75 | Re | Rhenium | Übergangsmetall | 186,21 |
| 76 | Os | Osmium | Übergangsmetall | 190,23 |
| 77 | Ir | Irdium | Übergangsmetall | 192,22 |
| 78 | Pt | Platin | Übergangsmetall | 195,08 |
| 79 | Au | Gold (Aurum) | Übergangsmetall | 196,97 |
| 80 | Hg | Quecksilber (Hydrargyrum) | Übergangsmetall | 200,59 |
| 81 | Tl | Thallium | Metall | 204,38 |
| 82 | Pb | Blei (Plumbum) | Metall | 207,2 |
| 83 | Bi | Bismut (auch Wismut) | Metall | 208,98 |
| 84 | Po | Polonium | Metall | 209,98 |
| 85 | At | Astat | Halogen | 209,99 |
| 86 | Rn | Radon | Edelgas | 222,02 |
| 87 | Fr | Francium | Alkalimetall | 223,02 |
| 88 | Ra | Radium | Erdalkalimetall | 226,03 |
| 89 | Ac | Actinium | Übergangsmetall | 227,03 |
| 90 | Th | Thorium | Actinoid | 232,04 |
| 91 | Pa | Protactinium | Actinoid | 231,04 |
| 92 | U | Uran | Actinoid | 238,03 |
| 93 | Np | Neptunium | Actinoid | 237,05 |
| 94 | Pu | Plutonium | Actinoid | 244,06 |
| 95 | Am | Americium | Actinoid | 243,06 |
| 96 | Cm | Curium | Actinoid | 247,07 |
| 97 | Bk | Berkelium | Actinoid | 247 |
| 98 | Cf | Californium | Actinoid | 251,08 |
| 99 | Es | Einsteinium | Actinoid | 252,08 |
| 100 | Fm | Fermium | Actinoid | 257,1 |
| 101 | Md | Mendelevium | Actinoid | 258 |
| 102 | No | Nobelium | Actinoid | 259 |
| 103 | Lr | Lawrencium | Actinoid | 260 |
| 104 | Rf | Rutherfordium | Übergangsmetall | 261,11 |
| 105 | Db | Dubnium | Übergangsmetall | 262,11 |
| 106 | Sg | Seaborgium | Übergangsmetall | 263,12 |
| 107 | Bh | Bohrium | Übergangsmetall | 262,12 |
| 108 | Hs | Hassium | Übergangsmetall | 265 |
| 109 | Mt | Meitnerium | unbekannt | 266 |
| 110 | Ds | Darmstadtium | unbekannt | 269 |
| 111 | Rg | Roentgenium | unbekannt | 272 |
| 112 | Cn | Copernicium | unbekannt | 277 |
| 113 | Nh | Nihonium | unbekannt | 287 |
| 114 | Fl | Flerovium | unbekannt | 289 |
| 115 | Mc | Moscovium | unbekannt | 288 |
| 116 | Lv | Livermorium | unbekannt | 293 |
| 117 | Ts | Tenness | unbekannt | 292 |
| 118 | Og | Oganesson | unbekannt | 293 |