Um dich für deine nächste Prüfung vorzubereiten, schauen wir uns nun eine beispielhafte Klausuraufgabe an:
Im Biologieunterricht hast du erfahren, dass die Schale eines gewöhnlichen Hühnereis auch aus Kalk, also 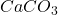 , besteht. Allerdings weißt du nicht, welchen Massenanteil das Kalziumkarbonat an der gesamten Hülle ausmacht. Daher entscheidest du dich kurzerhand, das selbst herauszufinden.
, besteht. Allerdings weißt du nicht, welchen Massenanteil das Kalziumkarbonat an der gesamten Hülle ausmacht. Daher entscheidest du dich kurzerhand, das selbst herauszufinden.
Du nimmst ein paar Eierschalenreste und mahlst sie zu einem feinen Pulver. Mit einer Waage erfährst du, dass deine Probe 15 Gramm wiegt. Anschließend übergießt du dieses mit einem Liter 0,5 molarer Salzsäure. Du siehst, wie Luftblasen aus deiner Lösung aufsteigen, was auf eine Gasentwicklung hindeutet. Danach wartest du ab, bis dieser Prozess abgeschlossen ist.
Aus dem Chemieunterricht weißt du, dass man die Stoffmenge der noch vorhandenen Salzsäure durch Titration mit einer Base bestimmen kann. Dafür gibst du eine 0,2 molare Natronlauge in die Lösung. Bis zum Erreichen des Äquivalenzpunktes verbrauchst du hierfür insgesamt 1,2 Liter.
Nun sollst du den Masseanteil an Kalziumkarbonat in deiner Eierschalenprobe berechnen.
Überlege hierfür zunächst, welche Schritte nacheinander durchgeführt werden, und was die Ergebnisse dieser sind. Das Aufstellen der relevanten Reaktionsgleichungen kann dir hierbei helfen.
Die Lösung und alle nötigen Rechenschritte und Überlegungen zeigen wir dir im Video !