Wie lässt sich eine Zerlegung von Wasser durch elektrischen Strom bewerkstelligen und welches Gerät kann dabei zum Einsatz kommen? Wenn du die Antworten auf diese Fragen erhalten möchtest, bist du hier genau richtig. Wir erklären dir die Elektrolyse von Wasser mit den zugehörigen Reaktionen und ihren Gleichungen. Außerdem erfährst du, was der Hofmannsche Zersetzungsapparat ist und wie er verwendet wird.
Du möchtest dich über die Wasserelektrolyse schnell und einfach in visueller Form informieren? Dann ist unser zugehöriges Video sicherlich die beste Wahl.
Inhaltsübersicht
Elektrolyse von Wasser einfach erklärt
Du kannst dir die Elektrolyse von Wasser als eine Zerlegung von Wasser in Sauerstoff und Wasserstoff durch elektrischen Strom vorstellen. Die Zerlegung erfolgt durch eine Redoxreaktion . Diese kannst du aufteilen in eine Oxidation an der mit dem Pluspol verbundenen Elektrode (Anode). Eine Oxidation kannst du dir als eine Elektronenabgabe des reagierenden Stoffes vorstellen. Die Elektronenaufnahme, also die Reduktion, findet an der mit dem Minuspol verbundenen Elektrode (Kathode) statt.
Elektrolyse
Grundsätzlich ist die Elektrolyse ein Prozess, bei dem elektrischer Strom eine chemische Stofftrennung erzwingt. Dabei kannst du jedoch nicht nur Wasser, sondern auch verschiedenste andere Stoffe in der Elektrolysezelle trennen.
Mehr zu der Elektrolyse und ihrer verschiedenen Anwendungsmöglichkeiten findest du in unserem entsprechenden Artikel .
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Elektrolyse von Wasser Reaktionsgleichungen
Durch die sogenannte Autoprotolyse des Wassers
liegt das Wasser nicht immer in seiner reinen Form vor und bildet Oxonium-Ionen ( ) und Hydroxid-Ionen (
) und Hydroxid-Ionen ( ). Wenn du nun eine Spannung anlegst, wandern die positiv geladenen Oxonium-Ionen (
). Wenn du nun eine Spannung anlegst, wandern die positiv geladenen Oxonium-Ionen ( ) im Elektrolyten zur Kathode. Dort können sie jeweils ein Elektron aufnehmen und es bilden sich neue Wasserstoffmoleküle (
) im Elektrolyten zur Kathode. Dort können sie jeweils ein Elektron aufnehmen und es bilden sich neue Wasserstoffmoleküle ( ).
).
Die negativen geladenen Hydroxide ( ) wandern zur Anode. Dort verbinden sie sich entweder mit Protonen (
) wandern zur Anode. Dort verbinden sie sich entweder mit Protonen ( ) zu Wasser (
) zu Wasser ( ) oder sie geben Elektronen ab und wandeln sich zu Sauerstoff (
) oder sie geben Elektronen ab und wandeln sich zu Sauerstoff ( ) um. Du kannst den entstandenen gasförmigen Wasserstoff und den Sauerstoff nun aus diesem Vorgang extrahieren.
) um. Du kannst den entstandenen gasförmigen Wasserstoff und den Sauerstoff nun aus diesem Vorgang extrahieren.
Kathode:
 oder
oder 
Anode:
 oder
oder 
Als Gesamtreaktion kannst du folgenden Zusammenhang formulieren:
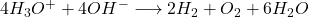
Durch den Zusammenhang der Autoprotolyse des Wassers lassen sich die Oxonium-Ionen ( ) und die Hydroxid-Ionen (
) und die Hydroxid-Ionen ( ) zu Wasser (
) zu Wasser ( ) zusammenfassen.
) zusammenfassen.
Dadurch erhältst du nach Ausgleichen für die Redoxreaktion:

Hofmannscher Zersetzungsapparat
Der Hofmannsche Zersetzungsapparat ist ein Gerät, in dem du eine Elektrolyse von Wasser durchführen kannst. Er wurde nach dem deutschen Chemiker August Wilhelm von Hoffmann benannt.
Das Gerät besteht aus drei miteinander kommunizierenden Röhren. Die mittlere Röhre wird so weit mit verdünnter Schwefelsäure gefüllt, bis die beiden äußeren Röhren komplett befüllt sind. Verdünnte Schwefelsäure ist eine Mischung aus Wasser und 10 bis 20% Schwefelsäure. Diese Mischung eignet sich besser für die Zerlegung von Wasser, da sie eine höhere elektrische Leitfähigkeit besitzt. Im unteren Teil der äußeren Röhren befinden sich Platinelektroden. Wenn du nun eine Spannung anlegst, bilden sich an den Elektroden Gasbläschen. An der Kathode entsteht darauf Wasserstoff und an der Anode Sauerstoff. Diese Endprodukte können aus den äußeren Rohren entnommen werden.


