Thermodynamische Systeme und Zustandsgrößen
Du hast dich schon öfter gefragt, wie man thermodynamische Systeme beschreibt und wie man ein geschlossenes System, ein offenes System und ein abgeschlossenes System voneinander abgrenzen kann? Hier erfährst du das Wichtigste zum Thema Thermodynamische Systeme.
Inhaltsübersicht
Was bedeutet geschlossenes System, offenes System und abgeschlossenes System?
Um die Grundlagen der Thermodynamik zu verstehen, überlegen wir uns als erstes, was thermodynamische Systeme sind. Per Definition ist das die Abgrenzung eines Bereichs für die thermodynamische Analyse, umschlossen von gedachten Systemgrenzen. Doch diese Definition zum Bereich Thermodynamische Systeme ist nicht besonders anschaulich. Deshalb betrachten wir einmal kochendes Wasser im Topf. Als thermodynamisches System können wir hier einfach das kochende Wasser selbst wählen und legen unsere Systemgrenzen darum. Das können wir dann später thermodynamisch analysieren. Du kannst dir bestimmt vorstellen, dass es immer vom Fall abhängig ist, ob es sich um ein geschlossenes System, ein offenes System oder ein abgeschlossenes System handelt. Wenn wir Eier ins Wasser legen, können wir auch die Systemgrenzen um das Ei legen, falls uns das Ei mehr interessiert.
Fassen wir das Ganze noch einmal zusammen:
- Thermodynamische Systeme sind die Abgrenzung eines Bereichs durch Systemgrenzen
- Es existieren geschlossene, abgeschlossene und offene Systeme
Geschlossenes System, abgeschlossenes System und offenes System
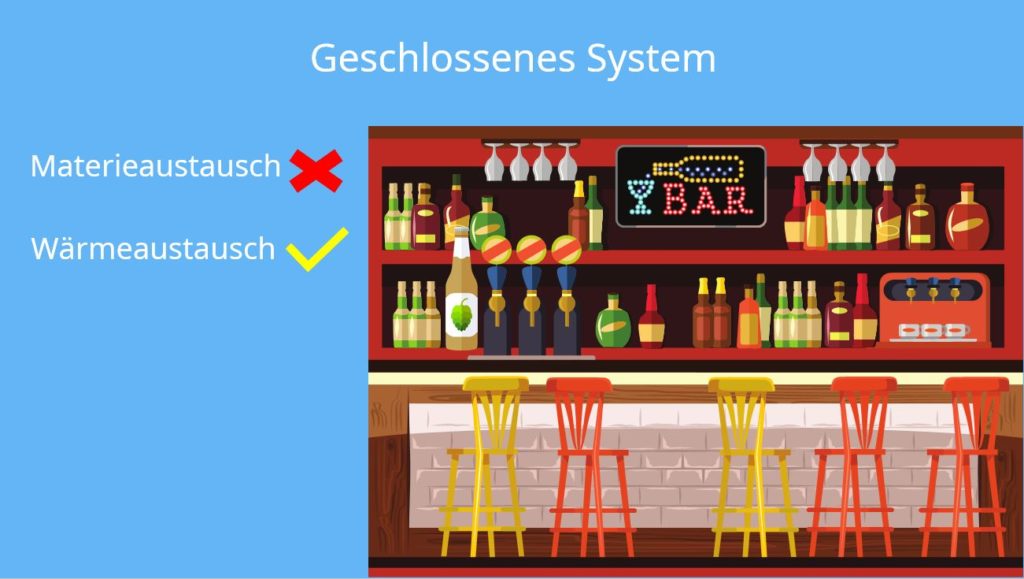
Bei der Wahl von thermodynamischen Systemen unterscheiden wir in drei Systeme: geschlossenes System, abgeschlossenes System und offenes System. Ein geschlossenes System ist materieundurchlässig, lässt aber einen Energieaustausch, zum Beispiel durch Wärme, zu. Dafür kannst du dir eine geschlossene Flasche Bier vorstellen. Wir können die Temperatur ändern, aber der Inhalt bleibt gleich.
Ein abgeschlossenes System hingegen lässt keinen Energieaustausch zu. Das ist der Fall, wenn du die Bierflasche isolierst, also kein Wärmeaustausch stattfinden kann. Du kannst dir jetzt sicher denken, dass sowohl ein Materie- als auch ein Energieaustausch zugelassen wird, sobald du die Bierflasche öffnest. Dies wird nun als offenes System bezeichnet.
Fluide Phasen und Reinstoffe
Wir wissen jetzt also, welche thermischen Systeme wir betrachten und wie wir ein geschlossenes System, ein offenes System und ein abgeschlossenes System jeweils voneinander abgrenzen können. Nun wollen wir thermische Systeme aber noch beschreiben können. In der Regel betrachten wir dazu fluide Phasen und sogenannte Reinstoffe. Fluide Phasen sind flüssig oder gasförmig. Das heißt: Alles, was sich zum Beispiel keiner Kuchenform anpasst, ist kein Fluid! Weiterhin zeichnen sich fluide Phasen dadurch aus, dass sie homogen verteilt und örtlich konstant sind. Beim kochenden Wasser nehmen wir also an, dass das Wasser überall „gleich“ kocht.
Und was sind jetzt Reinstoffe? Das ist eigentlich ganz einfach. Reinstoffe bestehen nur aus EINER Art von Atomen beziehungsweise Molekülen. Bei einem Gas zum Beispiel nur aus Wasserstoff, oder nur aus Sauerstoff. Luft ist – im Gegensatz dazu – ein Gasgemisch aus Stickstoff, Sauerstoff, Wasserstoff und einigen anderen Gasen.
Thermodynamische Systeme – Materie
Um diese Stoffe jetzt beschreiben zu können, verwenden wir sogenannte Zustandsgrößen: Materie, Volumen, Druck und Temperatur.
Bei der Materie können wir in Masse m und Stoffmenge n unterscheiden. Die Masse ist dir sicher bekannt und wird in Kilogramm angegeben. Die Stoffmenge kennst du vielleicht aus der Chemie und hat die Einheit Mol. Dabei sind in einem Mol 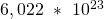 Atome, beziehungsweise Moleküle. Das heißt, die Stoffmenge ist ein Maß für die Anzahl der Teilchen. Die Masse wird meist verwendet, wenn die Zusammensetzung konstant bleibt.
Atome, beziehungsweise Moleküle. Das heißt, die Stoffmenge ist ein Maß für die Anzahl der Teilchen. Die Masse wird meist verwendet, wenn die Zusammensetzung konstant bleibt.
Also wenn wir ein Glas Wasser als ein thermisches System betrachten und nichts dazu schütten. Sobald wir irgendetwas in das Wasser geben, bietet es sich mehr an, die Stoffmenge zu verwenden. Auch wenn wir Reaktionen betrachten, verwenden wir die Stoffmenge. Zwischen Masse und Stoffmenge gibt es einen stoffspezifischen Zusammenhang: die sogenannte Molmasse:
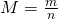
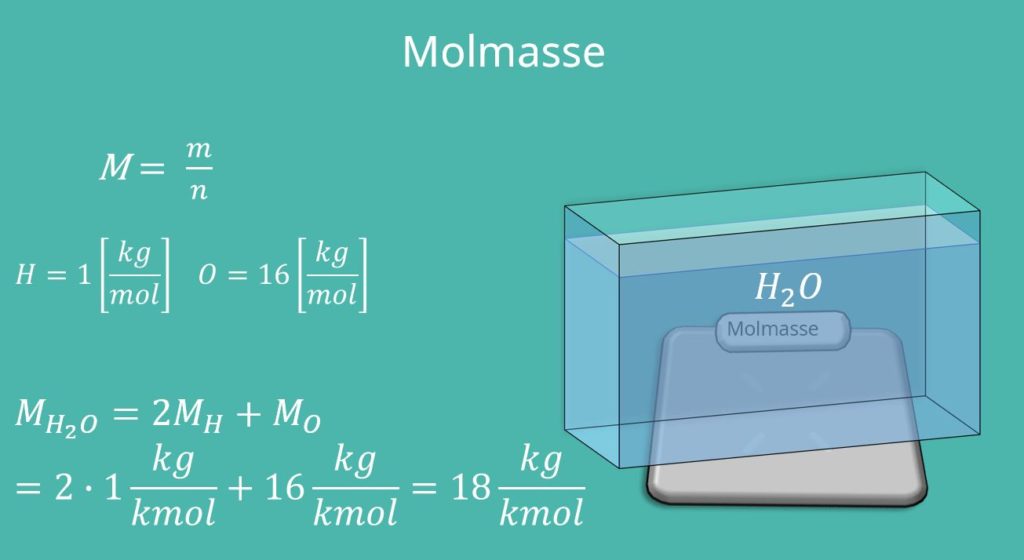
Diese gibt an, wie viel Kilogramm ein Kilomol eines bestimmen Stoffes wiegt. Das ist für jedes Element im Periodensystem angegeben. Um die Molmasse für ein Molekül zu bestimmen, addieren wir einfach die Molmassen der einzelnen Elemente. Rechnen wir das jetzt für Wasser – also 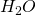 – durch: Wasserstoff hat eine Molmasse von 1 und Sauerstoff eine Molmasse von 16 Kilogramm pro Kilomol. Damit erhalten wir für Wasser eine Molmasse von:
– durch: Wasserstoff hat eine Molmasse von 1 und Sauerstoff eine Molmasse von 16 Kilogramm pro Kilomol. Damit erhalten wir für Wasser eine Molmasse von:
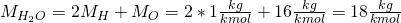
Thermodynamische Systeme – Volumen und Druck
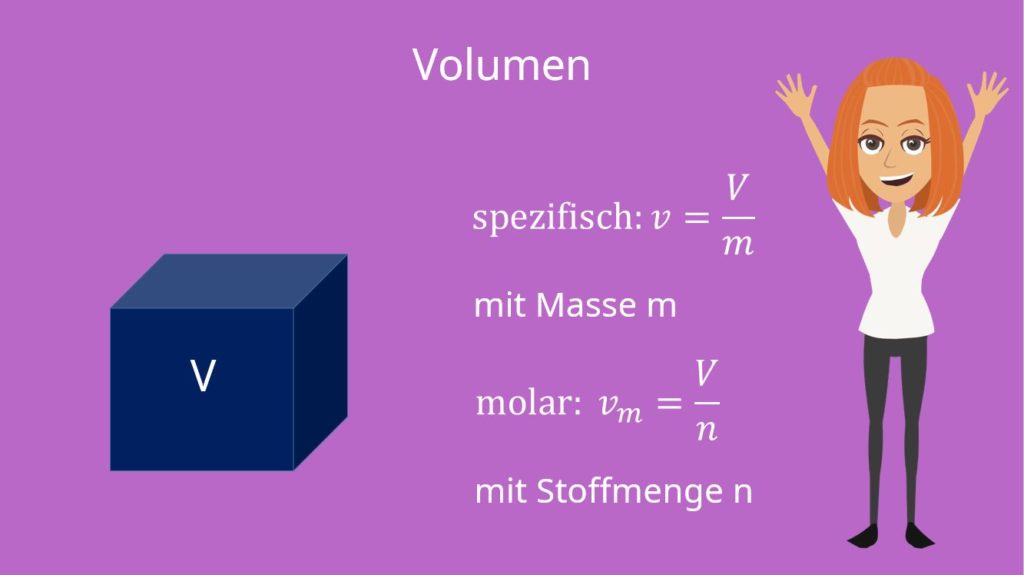
Das Volumen V, welches in Kubikmeter angegeben wird, kennst du sicher auch. Oft betrachten wir aber das spezifische, beziehungsweise molare Volumen, je nachdem, ob wir die Masse oder die Stoffmenge betrachten wollen.
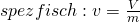
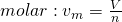
Das spezifische Volumen bildet dabei einfach den Kehrwert der Dichte Roh:
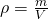
Der Druck p kommt dir sicher auch bekannt vor und wird in Pascal angeben. Wahrscheinlich kennst du die Einheit Bar besser. Ein Bar entspricht dabei 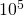 Pascal.
Pascal.
Nun weißt du, was thermodynamische Systeme sind und wie man ein geschlossenes System, ein offenes System und ein abgeschlossenes System gegeneinander abgrenzt.