Wie lauten die Hauptsätze der Thermodynamik und was steckt dahinter? In diesem Beitrag erklären wir sie dir!
Inhaltsübersicht
Die Hauptsätze der Thermodynamik einfach erklärt
Die Thermodynamik (Wärmelehre) ist ein Teilgebiet der Physik. Sie beschäftigt sich mit der Umwandlung und Änderung von Energie innerhalb eines oder mehrerer Systeme.
Die wichtigsten Grundprinzipien werden in den Hauptsätzen der Thermodynamik zusammengefasst. Insgesamt gibt es vier Hauptsätze, die von null bis drei durchnummeriert sind. Alle bauen aufeinander auf und ergänzen sich gegenseitig. Hier siehst du alle Hauptsätze der Thermodynamik auf einen Blick:
- 0. Hauptsatz: Gesetz des thermischen Gleichgewichtes
- 1. Hauptsatz: Energieerhaltungssatz der Thermodynamik
- 2. Hauptsatz: Entropiesatz der Thermodynamik
- 3. Hauptsatz: Nernschtes Wärmetheorem
Häufig ist fälschlicherweise von 3 Hauptsätzen die Rede. Das liegt daran, dass der nullte Hauptsatz erst später hinzugefügt wurde. Aufgrund seiner Wichtigkeit steht er den anderen Hauptsätzen der Thermodynamik an nullter Stelle voraus.
Hauptsätze der Thermodynamik – 0. Hauptsatz
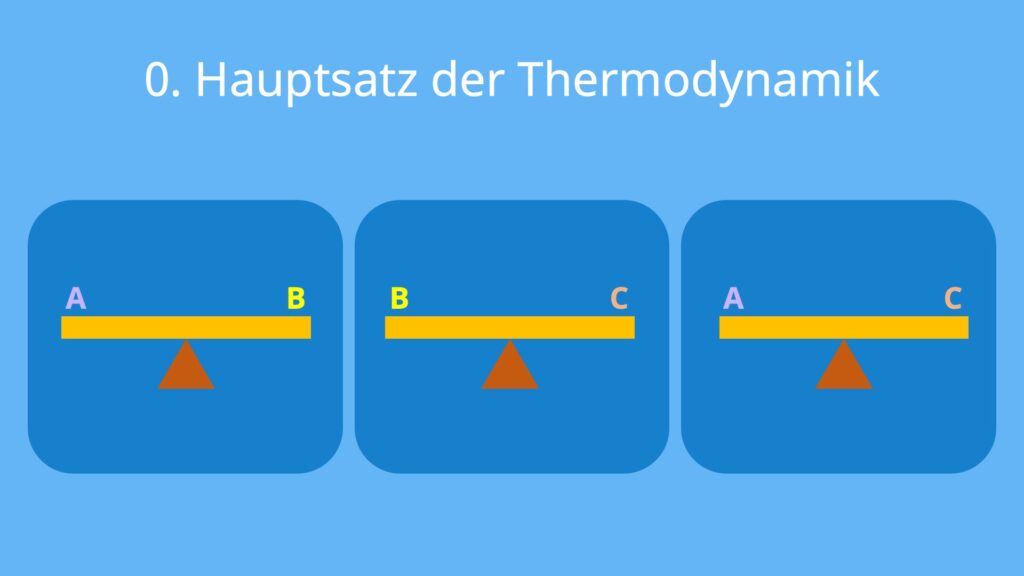
Der nullte Hauptsatz der Thermodynamik (Gesetz des thermischen Gleichgewichtes) sagt aus, dass zwei Systeme, die im Energieaustausch zueinander stehen, immer einen thermodynamischen Gleichgewichtszustand anstreben. Das heißt, dass sich die Zustände der Systeme in Bezug auf Temperatur, Druck und Volumen angleichen.
Stell dir vor, die Systeme A und B stehen im Gleichgewicht zueinander. Außerdem ist das System B mit einem dritten System C gekoppelt. Folglich stehen die Systeme A und C ebenfalls im thermodynamischen Gleichgewicht.
So lässt sich aus dem nullten Gesetz der Thermodynamik zusätzlich die Aussage ableiten: Ein drittes System steht auch mit den beiden anderen Systemen im thermodynamischen Gleichgewicht, sobald es an eines der Systeme gekoppelt wird.
Wenn du mehr über den nullten Hauptsatz der Thermodynamik erfahren willst, dann schau dir unser Video dazu an!
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Hauptsätze der Thermodynamik – 1. Hauptsatz
Der 1. Hauptsatz der Thermodynamik besagt, dass Energie weder erschaffen noch vernichtet werden kann. Energie lässt sich nur in verschiedene Formen umwandeln oder übertragen. In einem geschlossenen System ist die Energie deshalb immer konstant. Deshalb nennst du den 1. Hauptsatz auch Energieerhaltungssatz.
Anders formuliert, besagt das 1. Grundprinzip, dass die Änderung der inneren EnergieΔE eines Systems gleich die Summe der verrichteten Arbeit ΔW und der frei werdenden Wärme ΔQ ist:
ΔE = ΔW + ΔQ
- Die innere Energie beschreibt die Gesamtenergie eines Systems.
- Die Wärmeenergie ist ein Maß für die Bewegung der Teilchen eines Stoffes. Je schneller sich die Teilchen bewegen, desto wärmer ist der Stoff.
Beispiel: Stell dir einen Topf mit Wasser vor. Indem du das Wasser im Topf umrührst, verrichtest du Arbeit an dem System und erhöhst somit dessen Gesamtenergie. Wenn also ΔWdurch dein Umrühren erhöht wird und ΔQ konstant bleibt, dann erhöht sich ΔE.
Übrigens: Du kannst die innere Energie eines Systems anstelle des ΔE auch mit ΔU darstellen. Beide Schreibweisen sind möglich.
Mehr über den Hintergrund des ersten Hauptsatzes der Thermodynamik erfährst du in unserem separaten Video zum Thema!
Hauptsätze der Thermodynamik – 2. Hauptsatz
Der 2. Hauptsatz der Thermodynamik (Entropiesatz der Thermodynamik) beschreibt, in welcher Form (Entropie, reversible, irreversible) und in welcher Richtung (bis gleich warm) Energie von einem zum anderen System übertragen wird. Das Prinzip ergänzt somit den ersten Hauptsatz, welcher besagt, dass Energie übertragen werden kann.
Übertragung von Energie ist nicht zu 100% möglich
Du kannst Arbeit immer in Wärme umwandeln. Zum Beispiel, wenn du die Hände aneinander reibst, entsteht Reibungswärme. Umgekehrt kannst du die Wärme jedoch nicht zu 100 % wieder in Arbeit überführen. Es gibt immer Verluste und nur ein Teil lässt sich umwandeln. Der Prozess ist daher irreversibel, weil er nicht wieder vollständig umkehrbar ist.
Richtung der Energieübertragung
Außerdem besagt der 2. Hauptsatz, dass die Energieübertragung immer nur in eine bestimmte Richtung abläuft: vom warmen zum kalten Objekt. Das lässt sich durch die Entropie
erklären.
Du nennst die Entropie auch die Unordnung eines Systems. Je höher die Entropie eines Systems ist, desto mehr Anordnungsmöglichkeiten der enthaltenen Teilchen gibt es. Energie fließt dabei immer nur in die Richtung, in der sie die Entropie erhöht.
Beispiel: Wenn du beispielsweise deine Hand in kaltes Wasser hältst, dann wird die Wärmeenergie immer von deiner warmen Hand zum kälteren Wasser übertragen. Die Übertragung läuft so lange, bis beide Systeme die gleiche Temperatur erreicht haben.
Die Details des zweiten Hauptsatzes erklären wir dir in unserem eigenen Video dazu!
Hauptsätze der Thermodynamik – 3. Hauptsatz
Der dritte Hauptsatz der Thermodynamik besagt, dass ein Stoff nicht auf den absoluten Nullwert abgekühlt werden kann.
Der absolute Nullpunkt (-273 °Celsius = 0 Kelvin) ist die theoretisch tiefstmögliche Temperatur. Hier kommen die Teilchen eines Stoffes zum vollständigen Stillstand und es kann auch keine Entropieänderungen mehr geben.
Das wäre in der Theorie allerdings nur bei perfekten Kristallen mit unendlicher Ausdehnung möglich. Sobald die Gitterstruktur des Kristalls einen Fehler oder einen Bruch aufweisen würde, hätte ein Teilchen mehr Platz als die anderen. Damit wäre auch seine Entropie größer.
Der perfekte Kristall ist allerdings nur eine theoretische Vorstellung. Denn Flüssigkeiten frieren in der Regel so ein, wie sie auch im flüssigen Zustand vorliegen — meist wild durchmischt. Auch die unendliche Ausdehnung kann in Wirklichkeit nicht existieren.
Somit kann sich ein Stoff zwar dem absoluten Nullpunkt annähern, ihn jedoch nie erreichen. Dadurch lässt sich der wahre Entropiewert an diesem Punkt nie bestimmen. Aus diesem Grund wurde der Entropiewert willkürlich für den absoluten Nullpunkt auf 0 gesetzt. Das hat den Vorteil, dass sich nun andere Entropien in Bezug auf den Zustand beim absoluten Nullpunkt messen lassen.
Wenn du noch mehr über den dritten Hauptsatz lernen willst, dann schau dir unser Video dazu an!
Hauptsätze der Thermodynamik — häufigste Fragen
(ausklappen)
Hauptsätze der Thermodynamik — häufigste Fragen
(ausklappen)-
Warum braucht man den 0. Hauptsatz überhaupt, wenn ich Temperatur schon „kenne“?Du brauchst den 0. Hauptsatz, weil er Temperatur überhaupt erst eindeutig definierbar macht. Er sagt, dass „gleiche Temperatur“ eine transitive Beziehung ist: Wenn A mit B im Gleichgewicht ist und B mit C, dann auch A mit C. Genau das rechtfertigt Thermometer als Vergleichssystem.
-
Was zählt in Thermodynamik-Aufgaben eigentlich als Systemgrenze, wenn sich das System bewegt oder verformt?Die Systemgrenze ist die gedachte Trennfläche, über die Wärme, Arbeit oder Masse das System verlassen oder eintreten. Bei Bewegung oder Verformung wählst du meist eine mitbewegte, materielle Grenze (geschlossenes System) oder eine feste Kontrollfläche im Raum (Kontrollvolumen). Beispiel: Turbine nutzt fast immer ein Kontrollvolumen.
-
Wie entscheide ich in einer Aufgabe, ob ich für den 1. Hauptsatz innere Energie oder Enthalpie benutzen muss?Du nutzt innere Energie bei geschlossenen Systemen und Enthalpie bei Strömungsprozessen mit Massenstrom. Der Grund ist, dass bei Ein- und Ausströmung die sogenannte Strömungsarbeit
 automatisch in der Enthalpie
automatisch in der Enthalpie  steckt. Beispiel: Kolben-Zylinder eher
steckt. Beispiel: Kolben-Zylinder eher  , Düse eher
, Düse eher  .
.
-
Wie finde ich in einer Aufgabe heraus, ob die Entropie des Systems wirklich abnimmt, obwohl der 2. Hauptsatz gilt?Ja, die Entropie eines Systems kann abnehmen, wenn genügend Entropie an die Umgebung abgegeben wird. Prüfe dazu die Entropiebilanz:
 , wobei
, wobei  . Beispiel: Beim Abkühlen mit Wärmeabgabe ist
. Beispiel: Beim Abkühlen mit Wärmeabgabe ist  möglich.
möglich.
-
Welche Fehler passieren oft, wenn ich den 3. Hauptsatz auf reale Stoffe anwende, die kein perfekter Kristall sind?Ein häufiger Fehler ist, für reale Stoffe einfach
 anzunehmen, obwohl sie Restentropie durch Unordnung behalten können. Außerdem wird oft vergessen, dass Phasenübergänge und Wärmekapazitäten bis nahe 0 K in die Entropieberechnung eingehen. Unüblich, aber nicht „falsch“, sind vereinfachte Näherungen, wenn sie begründet sind.
anzunehmen, obwohl sie Restentropie durch Unordnung behalten können. Außerdem wird oft vergessen, dass Phasenübergänge und Wärmekapazitäten bis nahe 0 K in die Entropieberechnung eingehen. Unüblich, aber nicht „falsch“, sind vereinfachte Näherungen, wenn sie begründet sind.
Perpetuum Mobile
Das Perpetuum Mobile ist eine theoretische Maschine, die mehr Energie erzeugt als sie verbraucht. Warum sie nur in der Theorie existiert und wie sie den Hauptsätzen der Thermodynamik widerspricht, erfährst du in unserem Video !