Thermodynamisches Gleichgewicht
Wie du weißt herrscht ein Gleichgewicht immer dann, wenn sich ein System nicht mehr weiter ändert. In diesem Beitrag geht es um das Gleichgewicht in thermodynamischen Systemen.
Inhaltsübersicht
Abgrenzung von thermodynamischen Systemen und die drei verschiedenen Arten von Gleichgewichten
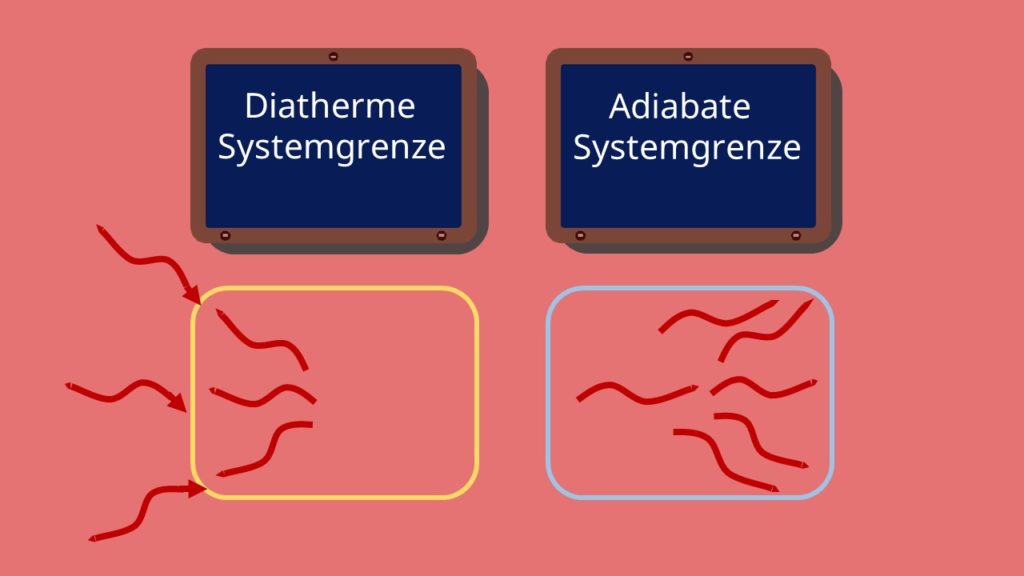
Ein System kann in der Thermodynamik durch zwei Systemgrenzen von seiner Umgebung isoliert sein. Eine diatherme Systemgrenze ist wärmedurchlässig. Eine adiabate Systemgrenze dagegen ist wärmeundurchlässig.
Nach einer Störung von außen kehren die meisten Systeme nach einiger Zeit wieder in einen Gleichgewichtszustand zurück.
Stell dir zunächst einen Luftballon vor. Im Inneren des Ballons herrscht ein höherer Druck als in der Umgebungsluft.
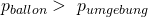
Wenn du nun ein Loch in den Ballon machst, strömt die Luft aus dem Ballon aus und ein Zustand des Gleichgewichts wird angestrebt.
Nach kurzer Zeit entspricht der Druck im Ballon dem der Umgebung.
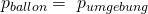
Wir unterscheiden im Allgemeinen zwischen einem mechanischen, chemischen und thermischen Gleichgewicht.
Erklärung zum mechanischen Gleichgewicht
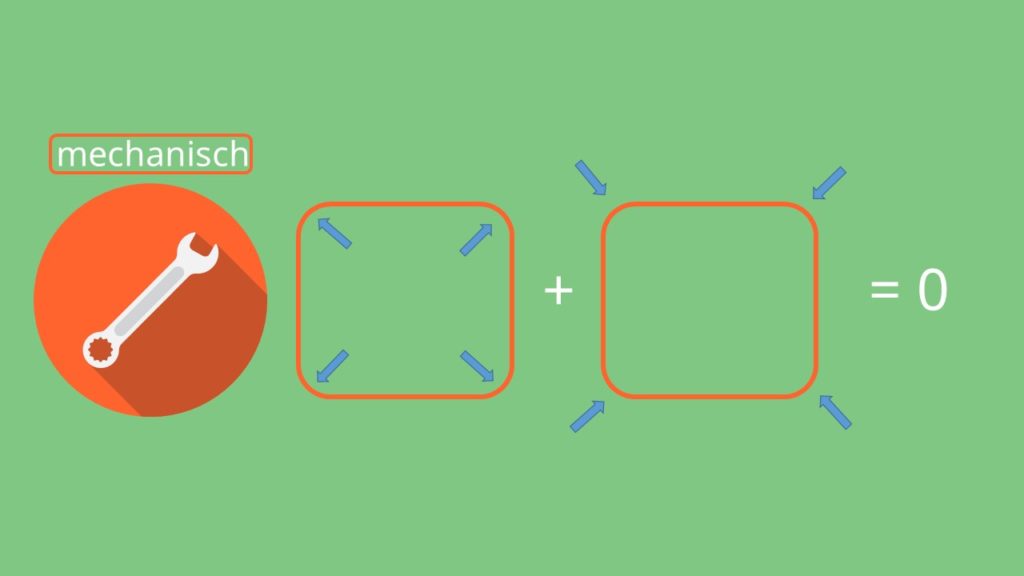
Das mechanische Gleichgewicht ist dann erreicht, wenn sich die Summe aller internen und externen Krafteinwirkungen zu Null kompensieren.
Also wenn jede Bewegung durch Reibung unterbunden wird und sich das System am Minimum der potentiellen Energie befindet.
Das chemische Gleichgewicht
Wenn du zum Beispiel Salz in Wasser auflöst, sprechen wir von einem chemischen Gleichgewicht, sobald das Wasser gesättigt ist und sich die Zahl der gelösten Ionen nicht mehr ändert. Die Teilchenzahl ändert sich also nicht mehr.
Das thermische Gleichgewicht
Zu guter Letzt gibt es noch das thermische Gleichgewicht. Es setzt voraus, dass sowohl alle Teile innerhalb des diathermisch getrennten Systems, als auch die Umgebung selbst die gleiche Temperatur haben.
Wenn du also dein Bier in den Kühlschrank stellst und dieses nach einiger Zeit die Temperatur der Umgebungsluft annimmt, findet kein weiterer Wärmefluss mehr statt. Es herrscht ein thermisches Gleichgewicht.
Das thermodynamische Gleichgewicht als Zusammenfassung der drei Untergleichgewichte
Das thermodynamische Gleichgewicht umfasst alle diese drei Unterpunkte und setzt voraus, dass keine weiteren Veränderungen an den Zustandsvariablen, wie Temperatur, Druck oder Teilchenanzahl auftreten.
So, nun kennst du die verschiedenen Gleichgewichtszustände in der Thermodynamik und weißt wann diese erreicht sind. Viel Erfolg.