Aus welchen Verbindungen besteht ein Peptid und wie kann man Peptide einteilen? In diesem Artikel erklären wir dir, was ein Peptid ist, wie es aufgebaut ist und wie du sie nach Anzahl ihrer Aminosäuren einteilen kannst.
Schau dir auch gerne unser Video dazu an, wenn du die Peptide schnell und einfach erklärt haben möchtest.
Inhaltsübersicht
Peptid einfach erklärt
Grundsätzlich ist ein Peptid ein aus Aminosäuren aufgebautes Molekül. Sogenannte Peptidbindungen verknüpfen diese Aminosäuren zu großen Ketten. Die Einteilung dieser Peptide kannst du je nach Anzahl der Aminosäuren, aus denen sie aufgebaut sind und je größer damit die Peptidkette wird, durchführen. Peptide kommen in allen Organismen vor und sorgen dabei für unterschiedliche Funktionen. So können sie unter anderem als Neurotransmitter, Peptidhormon oder als Antibiotika auftreten.
Struktur
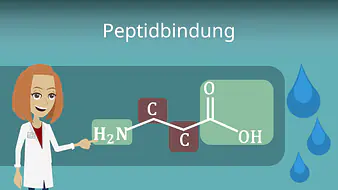
Peptide bilden sich bei einer Kondensationsreaktion der  – Carboxygruppe (
– Carboxygruppe ( ) einer Aminosäure und der
) einer Aminosäure und der  – Aminogruppe (
– Aminogruppe ( ) einer weiteren Aminosäure.
) einer weiteren Aminosäure.
Unser Artikel zur Peptidbindung
gibt dir einen Überblick über diese Verbindung und definiert die Bedeutung von  .
.
Die daraus entstehende Säureamidgruppierung ( ) (=Peptidgruppe) ist kennzeichnend für ein Peptid. Die freie Carboxygruppe am Ende des Petids wird als C-Terminus und die freie Aminogruppe am anderen Ende als N-Terminus bezeichnet.
) (=Peptidgruppe) ist kennzeichnend für ein Peptid. Die freie Carboxygruppe am Ende des Petids wird als C-Terminus und die freie Aminogruppe am anderen Ende als N-Terminus bezeichnet.
Je nachdem, wie lang diese Kette an Aminosäuren ist, kannst du ein Peptid in unterschiedliche Bereiche einteilen.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Dipeptid
Dipeptide werden dabei aus zwei Aminosäureresten zusammengesetzt. Dabei erfolgt die Benennung eines Dipeptids anhand der beiden Aminosäuren. Wenn beide Aminosäuren identisch sind, wird der Name der Animosäure dem Namen vorangestellt: Alanylalanin, Serylserin. Bei unterschiedlichen Aminosäuren musst du zuerst die Aminosäure mit der freien Carboxygruppe suchen, also den C-Terminus. Diese liefert dir den Stammnamen für deine Verbindung. Der Aminosäurerest mit dem N-Terminus wird diesem Namen vorangestellt. So können bei einer Verbindung der Aminosäuren Glycin (Gly) und Alanin (Ala) das Dipeptid Alanylglycin (Ala-Gly) oder Glycylalanin (Gly-Ala) entstehen.
Die Dipeptide entstehen im Körper meist als Zwischenprodukte bei der enzymatisch gesteuerten Verdauung von Proteinen.
Tripeptid
Tripeptide bestehen grundsätzlich aus einer Verbindung von drei Aminosäure-Resten. Die Benennung erfolgt ähnlich zu den Dipeptiden, indem die C-terminale Aminosäure als Stammname verwendet und die N-terminale Aminosäure vorangestellt wird. Die dritte Aminosäure wird bei der Benennung zwischen diesen beiden anderen Aminosäuren eingeordnet. Das beispielhafte Tripeptid Glutathion (=Glutamylcysteinylglycin) besteht aus den drei Aminosäuren Glutaminsäure, Cystein und Glycin.
Oligopeptid
Als Oligopeptid kannst du Peptide bezeichnen, die durch weniger als zehn Aminosäuren miteinander verknüpft sind. Somit zählen die Dipeptide und die Tripeptide auch zu den Oligopeptiden. Sie spielen in unserem Körper meist als Enzyme bei Entgiftungs– oder Stoffwechselprozessen eine Rolle.
Cyclopeptid
Ein ringförmiges Peptid wird als Cyclopeptid oder Lactam bezeichnet. Cyclopeptide, die aus zwei Ringen bestehen, kannst du als bicyclische Peptide bezeichnen. Bekannte Vertreter dieser Gruppe sind das Phalloidin und das Amanitin. Aufgrund ihrer Form sind Lactame meist weniger beweglich als andere Peptide, sie weisen jedoch meist eine höhere Stabilität gegenüber Temperaturen auf.
Polypeptid
Ein Polypeptid ist ein Peptid, das aus zehn oder mehr Peptidbindungen durch Aminosäuren besteht. Polypeptide können natürlichen Ursprungs sein oder auch synthetisch hergestellt werden. Wenn die Polypeptidkette mehr als hundert Aminosäuren beinhaltet, spricht man von einem Makropeptid. Wenn dieses Makropeptid auch noch durch Wasserstoff- oder Disulfidbrücken verbunden ist, kannst du es als Protein bezeichnen.
Übersicht Peptide
Hier siehst du alle Peptide in der Übersicht:
| Bezeichnung | Anzahl Aminosäuren |
| Dipeptid | 2 |
| Tripeptid | 3 |
| Tetrapeptid | 4 |
| Pentapeptid | 5 |
| Hexapeptid | 6 |
| Heptapeptid | 7 |
| Octapeptid | 8 |
| Nonapeptid | 9 |
| Oligopeptid | unter 10 |
| Polypeptid | über 10 |
| Makropeptid | über 100 |
Vorkommen
Peptide kommen in allen Organismen vor, die Zellen besitzen. Dabei agieren sie vor allem als Hormone. Nachfolgend werden einigen wichtige Peptide und deren Funktion aufgelistet.
Das Peptid mit Namen ANP (Atriales natriuretisches Peptid) ist beispielsweise ein Peptidhormon, das von den Muskelzellen und des Herzvorhofes ausgeschüttet wird. Es dient dazu, den Salz- und Wasserhaushalt und damit den Blutdruck zu regulieren. Es besteht aus 28 Aminosäuren und zählt damit zu den Polypeptiden.
Ein weiteres wichtiges Peptid ist das Vasoaktive intestinale peptid (VIP). Dieses besteht ebenfalls aus 28 Aminosäuren und ist auch ein Hormon. VIP wird vermehrt im Verdauungstrakt gefunden und dient unter anderem dazu, die Blutgerinnung zu stoppen und die Verdauung zu regulieren.
Das Peptid YY (PYY) ist ein Hormon, das aus 36 Aminosäuren besteht. Beim Menschen kommt dies meist im Dünndarm vor. Durch Einnahme fettreicher Nahrung bildet sich vermehrt PYY und kann unter anderem die Geschwindigkeit der Magenentleerung verändern, was das Sättigungsgefühl steigern kann.
C Peptid
Das C-Peptid (eng. connecting peptide) ist ein Spaltprodukt, das von dem primären Peptid Proinsulin bei dessen Umwandlung zu Insulin abgespalten wird. Daraufhin wird es zusammen mit dem Insulin aus den Zellen der Bauchspeicheldrüse in das Blut abgegeben. Da das C Peptid eine längere Halbwertszeit als Insulin besitzt, wird es als labordiagnostischer Parameter verwendet. Dieser Parameter zeigt die aktuelle Insulinabgabe der Bauchspeicheldrüse somit besser an, als eine Messung des Insulins selbst. Außerdem erfolgt keine Verzerrung des Wertes aufgrund möglicher Antikörper gegen Insulin. Durch die Messung der C-Peptid-Konzentration im Körper können beispielsweise Typ-1 und Typ-2 Diabetes unterschieden werden, ein Verdacht auf Insulinresistenz festgestellt werden oder eine Stoffwechselerkrankung gemessen werden. Weiterhin kann das C Peptid Effekte auf den Kohlenhydratstoffwechsel und auf die Vermeidung von Organschäden haben.
Anwendung
Peptide kommen sehr häufig in kosmetischen Produkten vor. Ihnen wird nachgesagt, gegen Hautalterung und Falten zu helfen. Grundsätzlich können Peptide die Kollagenproduktion im Körper vorantreiben. Kollagen ist ein Strukturprotein, das sich hauptsächlich im Bindegewebe befindet. Weiterhin kommt es in Knochen, Sehnen, Bändern und Knorpeln vor. Die Verabreichung erfolgt meistens intravenös, da die Haut einen natürlichen Abwehrmechanismus gegenüber Fremdstoffen, wie dem Peptid, besitzt. Ein weiterer Nachteil der Peptide besteht darin, dass sie von der Leber und den Nieren verhältnismäßig schnell abgebaut. Dadurch können sie ihre vermeintlich positiven Wirkungen oft nicht schnell genug entfalten. Meistens kann der Transport von Peptiden, aufgrund ihrer hydrophilen Eigenschaften im Körper, nicht ungehindert erfolgen.