Was sind Kohlenwasserstoffe und welche gibt es? Das erklären wir dir in unserem Video und folgendem Beitrag!
Inhaltsübersicht
Kohlenwasserstoffe einfach erklärt
Kohlenwasserstoffe sind eine Stoffgruppe, die nur aus Kohlenstoff- und Wasserstoffatomen bestehen. Sie gehören zu den vielfältigsten Stoffgruppen. Die häufigsten Vertreter sind aliphatische Kohlenwasserstoffe, also Alkane , Alkene , Alkine . Auch Aromate gehören zu den Kohlenwasserstoffen.
Insbesondere findest du Kohlenwasserstoffe im Erdgas und Erdöl, da sie als fossile Brennstoffe breite Anwendungsmöglichkeiten haben.
Unterteilung der Kohlenwasserstoffe
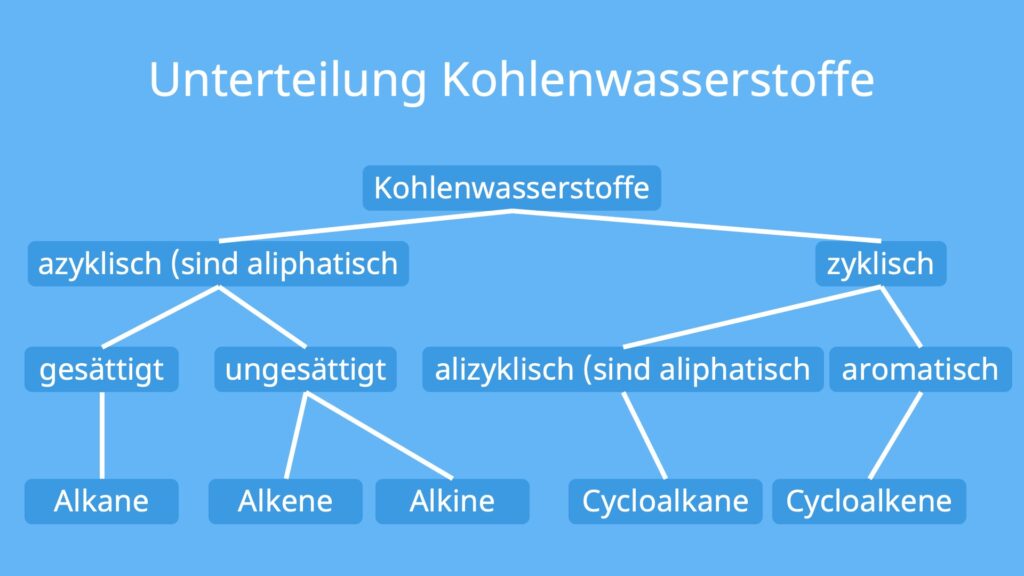
Du kannst die Kohlenwasserstoffe in azyklisch (kettenförmig) und zyklisch (ringförmig) unterteilen. Bei den azyklischen Kohlenwasserstoffen unterscheidest du zwischen gesättigt (Alkan) und ungesättigt (Alken und Alkin).
Zu den zyklischen gehören alizyklische (Cycloalkan und- alken) und aromatische Kohlenwasserstoffe. Als aliphatisch bezeichnest du alle Kohlenwasserstoffe, die nicht aromatisch sind. Aromatische Kohlenwasserstoffe hingegen erkennst du an mindestens einem aromatischen Ring .
Somit sind die Alkane, Alkene und Alkine sowie ihre zyklischen Formen (Cycloalkane und Cycloalkene) allesamt aliphatisch.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Alkane
Schauen wir uns als Erstes die Alkane an. Sie sind gesättigte Kohlenwasserstoffe und enthalten daher nur Einfachbindungen.
Alle Alkane enden namentlich auf -an. Anhand ihrer Anzahl an C-Atomen werden sie nach griechischen Zahlwörtern benannt (zum Beispiel Hexan hat 6 C-Atome).
Der einfachste Kohlenwasserstoff ist Methan (CH4). Fügst du jetzt zum Methan weitere CH2-Gruppen hinzu, dann erhältst du die homologe Reihe der Alkane. Im Folgenden siehst du eine Liste der einfachsten Alkane.
| Name | Summenformel | vereinfachte Strukturformel |
| Methan | CH4 | CH4 |
| Ethan | C2H6 | CH3-CH3 |
| Propan | C3H8 | CH3-CH2-CH3 |
| Butan | C4H10 | CH3-CH2-CH2-CH3 |
| Pentan | C5H12 | CH3-(CH2)3-CH3 |
| Hexan | C6H14 | CH3-(CH2)4-CH3 |
| Heptan | C7H16 | CH3-(CH2)5-CH3 |
| Octan | C8H18 | CH3-(CH2)6-CH3 |
| Nonan | C9H20 | CH3-(CH2)7-CH3 |
| Decan | C10H22 |
CH3-(CH2)8-CH3 |
Für die Alkane aus der homologen Reihe kannst du dir merken:
- Ihre allgemeine Form ist CnH2n+2.
- Sie sind alle unverzweigt.
- Die Siede- sowie Schmelzpunkte nehmen mit zunehmender Kettenlänge aufgrund der Van-der-Waals-Kräfte zu.
Alkene und Alkine
Alkene und Alkine gehören zu den ungesättigten Kohlenwasserstoffen und haben deshalb Mehrfachbindungen. Alkene enthalten dabei eine oder mehrere Doppelbindungen und enden auf -en. Alkine hingegen enthalten eine oder mehrere Dreifachbindungen und enden auf -in.
Ihre Namensgebung folgt den gleichen Regeln wie bei Alkanen. Außerdem gibt eine Zahl vor dem Namen des Alkens/Alkins die Stelle der Doppel- oder Dreifachbindung an. Zum Beispiel hat 1-Hexen eine Doppelbindung am ersten C-Atom und 4-Octin eine Dreifachbindung am vierten C-Atom.
Die einfachsten Alkene sind Ethen (C2H4), auch Ethylen genannt und Propen (C3H6) auch Propylen genannt. Die einfachsten Alkine sind Ethin (C2H2), auch Acetylen genannt, und Propin (C3H4), auch Methylacetylen genannt.
Auch bei den Alkenen und Alkinen gibt es eine homologe Reihe. Für Alkene nutzt du die allgemeine Formel CnH2n und für Alkine CnH2n-2.
Aromatische Kohlenwasserstoffe
Die aromatischen Kohlenwasserstoffe besitzen meistens sogenannte Arene, also C6-Ringe. Das sind 6 C-Atome in einem Ring angeordnet.
Damit eine Verbindung aber ein Aromat ist, muss sie
- zyklisch (Atome sind in einem Ring verbunden),
- planar (Atome sind flach angeordnet und liegen alle in der gleichen Ebene),
- durchkonjungiert (durchgehend benachbarte Doppelbindungen) sein und die
- Hückel-Regel erfüllen, also 4n+2 π-Elektronen haben.
Die einfachsten Vertreter der Aromaten sind Benzol (C6H6) und Toluol (H3C-C6H5).
Polyzyklische aromatische Kohlenwasserstoffe enthalten hingegen mehrere Ringe. Die bekanntesten Vertreter sind das Naphthalin (C10H8) sowie das Anthracen (C14H10).
Viele Farbstoffe haben vergleichbare Strukturen, in denen mehrere Ringe aneinander hängen.
Eigenschaften von Kohlenwasserstoffen
Durch ihre Vielfältigkeit besitzen Kohlenwasserstoffmoleküle verschiedene Eigenschaften.
- Sie sind hydrophob und lipophil. Dadurch lösen sie sich nicht in Wasser, sondern in unpolaren Lösungsmitteln.
- Bei gleicher Summenformel können Kohlenwasserstoffe unterschiedliche Strukturformeln aufweisen. Die Stoffe nennst du dann Isomere .
- Je länger und unverzweigter ein Kohlenwasserstoff ist, umso höher ist sein Siede- und Schmelzpunkt.
- Alkane sind wenig reaktiv, aber können H-Atome in Substitutionsreaktionen gegen andere Atome, zum Beispiel Halogene austauschen. Du sprichst dann von Halogenalkanen .
- Alkene und Alkine sind sehr reaktiv, weil sie durch ihre Mehrfachbindungen Additionsreaktionen durchführen können. Dabei spalten sie Mehrfachbindungen auf und können verschiedene Substanzen anbinden.
Vorkommen von Kohlenwasserstoffen
Kohlenwasserstoffverbindungen findest du fast überall. Schauen wir uns einige Beispiele an.
Alkane:
Alkane findest du meist im Benzin oder Kerosin als fossile Energieträger .
Alkene:
Alkene begegnen dir vor allem in der chemischen Industrie, da sie sehr oft Ausgangsstoffe für die Herstellung komplexerer Moleküle sind. Auch bei der Herstellung von Kunststoffen spielen sie eine große Rolle. Aus Ethen entsteht beispielsweise das Polyethylen, welches eines der am häufigsten verwendeten Kunststoffe auf der Welt ist.
Halogenkohlenwasserstoffe:
Also Beispiel für ein Halogenkohlenwasserstoff ist Trichlorfluormethan (CCl3F). Es wurde früher als Kältemittel eingesetzt. Genauer gesagt gehört es zu den Fluorchlorkohlenwasserstoffen (FCKW), welche heute als ozonschichtzerstörend eingestuft werden und deswegen verboten sind.
Chlorkohlenwasserstoffe kommen oft in Pflanzenschutzmitteln vor, aber auch in der Kunststoffchemie in Form des Polyvinylchlorids (PVC), welches du sicher aus Fußböden kennst.
Chloroform und Tetrachlormethan sind bedeutende Lösemittel in der Chemie. Chloroform wurde dabei früher auch als Narkosemittel eingesetzt und Tetrachlormethan als Feuerlöschmittel.
Aromatische Kohlenwasserstoffe:
Aus Toluol stellst du unter anderem den Sprengstoff Trinitrotoluol (TNT) her, welcher heute auch noch häufig genutzt wird. Darüber hinaus sorgt beispielsweise Benzol für den typischen „Benzingeruch“ an Tankstellen. Zudem ist Benzol ein bedeutender Ausgangsstoff für die Herstellung von Farbstoffen, Kunststoffen oder auch Insektiziden.
Radikalische Substitution
Jetzt hast du einen klaren Überblick über die Kohlenwasserstoffe erhalten. Möchtest du beispielsweise wissen, wie genau die Reaktion zu Chlorkohlenwasserstoff abläuft? Dann schau dir unser Video zur radikalischen Substitution an!