Die Hückel Regel hilft dir dabei, ein Aromat zu erkennen. Was sie besagt und wie genau du sie anwendest, erfährst du hier im Beitrag und im Video dazu.
Inhaltsübersicht
Hückel Regel einfach erklärt
Die Hückel Regel ist eine Regel der organischen Chemie und ein gutes Hilfsmittel, um Aromaten zu identifizieren. Die Regel besagt: Ein flaches, ringförmiges Molekül mit Doppelbindungen ist dann aromatisch, wenn es eine bestimmte Anzahl von konjugierten Elektronen enthält.
Um zu überprüfen, ob die bestimmte Anzahl der konjugierten Elektronen vorhanden ist, hilft dir folgende Formel:
4n+2 = π-Elektronen
Für n muss dabei eine natürliche Zahl herauskommen, wenn du für π-Elektronen die Anzahl der im Ring vorhandenen pi-Elektronen einsetzt.
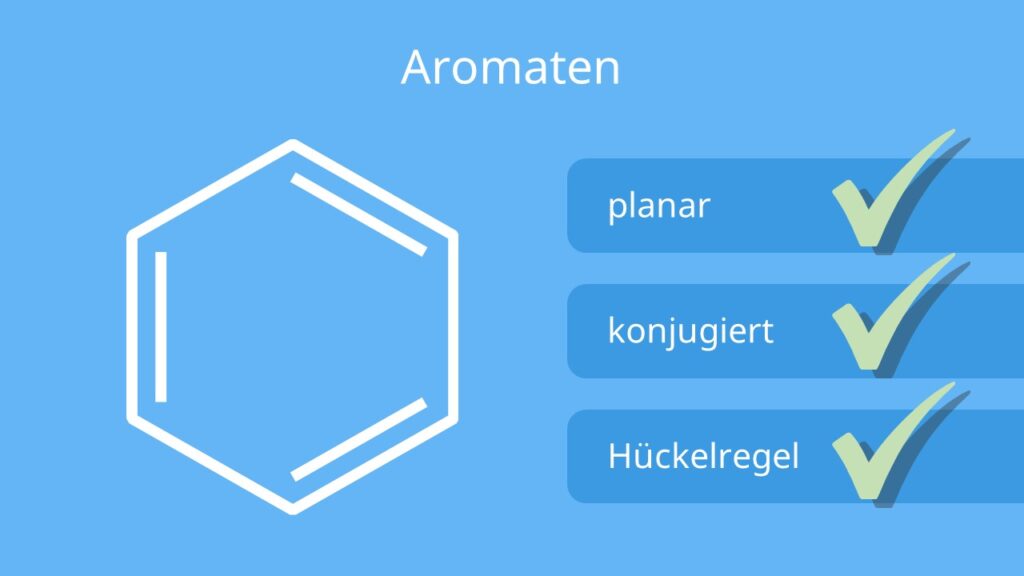
Aromaten sind äußerst stabile, ringförmige Kohlenwasserstoffe, die alle die drei folgenden Kriterien erfüllen:
- Planarität: Aromatische Verbindungen liegen planar vor. Das heißt alle Atome im Ring müssen flach in einer Ebene liegen.
- Konjugation: Aromatische Verbindungen müssen konjugiert sein. Das bedeutet, dass im Ringsystem gleichmäßig abwechselnd Doppel- und Einfachbindungen vorhanden sind.
- Hückel Regel: Aromatische Verbindungen erfüllen die Hückel-Regel.
Hückel Regel Anwendung
Um mit der Hückel Regel ein Aromat zu bestimmen, musst du folgende drei Schritte anwenden:
1. Schritt: Pi-Elektronen zählen
Zuerst zählst du die Anzahl der konjugierten pi-Elektronen im Ring. Das sind Elektronen, die sich in den P-Orbitalen eines Moleküls oder eines Atoms befinden.
P-Orbitale sind Orbitale, die durch eine Seitenbindung zwischen zwei benachbarten Atomen gebildet werden. Sie stellen in der Regel eine Doppelbindung oder eine Dreifachbindung dar.
Merke: Zähle alle Doppelbildungen, die im Ring vorhanden sind. Da jede Doppelbindung aus zwei Elektronen besteht, musst du die Anzahl der Zweifachbindungen verdoppeln, um die Anzahl der vorhandenen pi-Elektronen herauszufinden.
2. Schritt: Formel anwenden
Setze die Anzahl der pi-Elektronen mit folgender Formel gleich:
4n+2 = π-Elektronen
Wenn du zum Beispiel sechs pi-Elektronen hast, sieht deine Gleichung so aus:
4n+2 = 6
Jetzt kannst du n ausrechnen.
3. Schritt: N ausrechnen
Stelle deine Gleichung so um, dass du nach n auflösen kannst:
4n+2 = 6 |-2
4n = 4 |:4
n = 1
Wenn für n eine natürliche Zahl (1, 2, 3, 4,…) herauskommt, geht die Hückelregel auf. Das bedeutet, dass die Anzahl der pi-Elektronen im Ring gleich 4n+2 ist. Das Molekül ist somit aromatisch.
Wenn die Anzahl der pi-Elektronen nicht der Hückel-Regel entspricht, dann ist das Molekül nicht aromatisch. Es hat also nicht die gleiche Stabilität wie aromatische Verbindungen.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Heteroaromaten
Heteroaromaten sind organische Kohlenwasserstoff-Ringe, die aromatische Eigenschaften aufweisen. Der einzige Unterschied zu normalen Aromaten ist, dass im Ring mindestens ein Kohlenstoffatom durch ein anderes Atom (sog. Heteroatom) ersetzt wurde. Heteroatome sind in der Regel Stickstoff-, Sauerstoff- oder Schwefelatome.
Die Heteroaromaten unterscheiden sich allerdings darin, dass dieses Heteroatom durch seine freien Elektronenpaare zusätzliche pi-Elektronen beiträgt. Deshalb erhöht sich Gesamtzahl der pi-Elektronen im Ring. So hat zum Beispiel Furan 6 pi-Elektronen, da du das freie Elektronenpaar im Ring vom Sauerstoffatom mitzählst.
Fazit: Zähle bei Heteroaromaten auch die freien Elektronenpaare im Ring zu den pi-Elektronen.
Antiaromaten
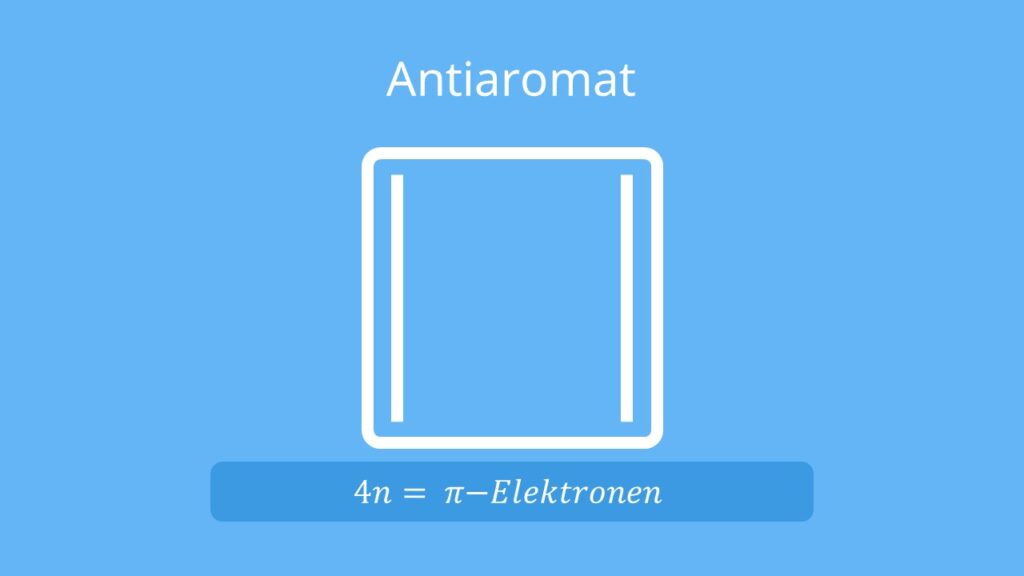
Bei Antiaromaten handelt es sich um Moleküle, die eine planare Konjugation von pi-Elektronen im Ring aufweisen, aber deren Gesamtzahl an pi-Elektronen nicht der Hückel Regel entspricht. Diese Moleküle sind aufgrund der unregelmäßigen Verteilung der pi-Elektronen energetisch instabil.
Fazit: Die Hückel-Regel kann bei Antiaromaten nicht angewendet werden. Stattdessen gilt für sie die Formel 4n = π-Elektronen.
Beispiele
Einige Beispiele für die Anwendung der Hückel Regel sind:
-
Benzol: Benzol ist ein sechsgliedriger Kohlenwasserstoff mit 6 pi-Elektronen in seinem konjugierten System. Nach der Hückel-Regel ist die Anzahl der pi-Elektronen in einem aromatischen Ring 4n+2, wobei n eine natürliche Zahl ist. Für Benzol ergibt das n=1.
-
Pyridin: Pyridin ist ein heteroaromatisches Molekül, das aus einem fünfgliedrigen Ring und einem Stickstoffatom besteht. Der Ring hat 6 pi-Elektronen im konjugierten System, was der Hückel-Regel entspricht. Das bedeutet, dass Pyridin aromatisch ist.
-
Cyclobutadien: Cyclobutadien ist ein viergliedriger Kohlenwasserstoff, der theoretisch antiaromatisch sein sollte. Er hat 4 pi-Elektronen im konjugierten System, was der Formel 4n entspricht und nicht der Hückel-Regel.
Hückel Regel — häufigste Fragen
-
Was ist die Hückelregel?
Die Hückelregel ist eine Regel der organischen Chemie. Sie besagt: Ein flaches, ringförmiges Molekül mit Doppelbindungen ist erst dann aromatisch, wenn es eine bestimmte Anzahl von konjugierten Elektronen enthält.
-
Was ist die Formel der Hückelregel?
Die Hückelregel lässt sich in folgender Formel aufschreiben:
4n+2 = π-Elektronen.
-
Bei welchen Stoffen funktioniert die Hückelregel?
Die Hückelregel funktioniert nur bei Aromaten und Heteroaromaten. Um Antiaromaten zu identifizieren, benötigst du folgende Formel:
4n = π-Elektronen.
Aromaten
Jetzt weißt du, wie du Aromaten mit der Hückel Regel identifizieren kannst. Schau jetzt in unseren Beitrag zu dem Thema, um mehr über ihre Besonderheiten und Reaktionsmechanismen zu erfahren. Bis gleich!