Alkene
Die Alkene sind ähnliche Verbindungen wie die Alkane und Alkine. Wir zeigen dir in unserem Beitrag und in unserem Video dazu, was genau Alkene sind.
Inhaltsübersicht
Alkene einfach erklärt
Alkene sind organische Verbindungen, welche nur aus Kohlenstoff- und Wasserstoffatomen bestehen (Kohlenwasserstoffe). Sie haben mindestens eine Doppelbindung zwischen zwei Kohlenstoffatomen, wobei die Position der Doppelbindung variieren kann.
Alkene findest du vor allem als Bestandteil in Erdöl und Erdgas. Sie sind durch ihre Doppelbindung ungesättigt. Doppelbindungen sind im Vergleich zu Einfachbindungen schwächer. Das ist der Grund, warum Alkene sehr reaktiv sind und zum Beispiel in der elektrophilen Addition oder Polymerisation verwendet werden.
Alle Alkene schreibst du mit der Endung -en (Beispielsweise Ethen oder Buten). Besonders ist, dass sich verschiedene Alkene nur in der Anzahl ihrer -CH2-Moleküle unterscheiden. Sie bilden deshalb die homologe Reihe der Alkene. Ihre allgemeine Summenformel schreibst du als CnH2n.
Alkane Alkene Alkine
Die Alkene gehört neben den Alkanen und Alkinen zu den aliphatischen Kohlenwasserstoffen. Genauer gesagt sind sie ungesättigte Kohlenwasserstoffe, da sie mindestens eine Doppelbindung besitzen.
Alkine sind ebenfalls ungesättigt, allerdings besitzen sie mindestens eine Dreifachbindung. Alkane hingegen sind gesättigt, das heißt, sie sind lediglich über Einfachbindungen verknüpft.
Die Alkene unterscheiden sich auch in ihrer Summenformel CnH2n von den Alkanen mit der Formel CnH2n+2 und den Alkinen mit der Formel CnH2n-2.
Alkene haben die Summenformel CnH2n. Das heißt, besitzt ein Alken eine Anzahl n Kohlenstoffatome, enthält es doppelt so viele (2 • n) Wasserstoffatome.
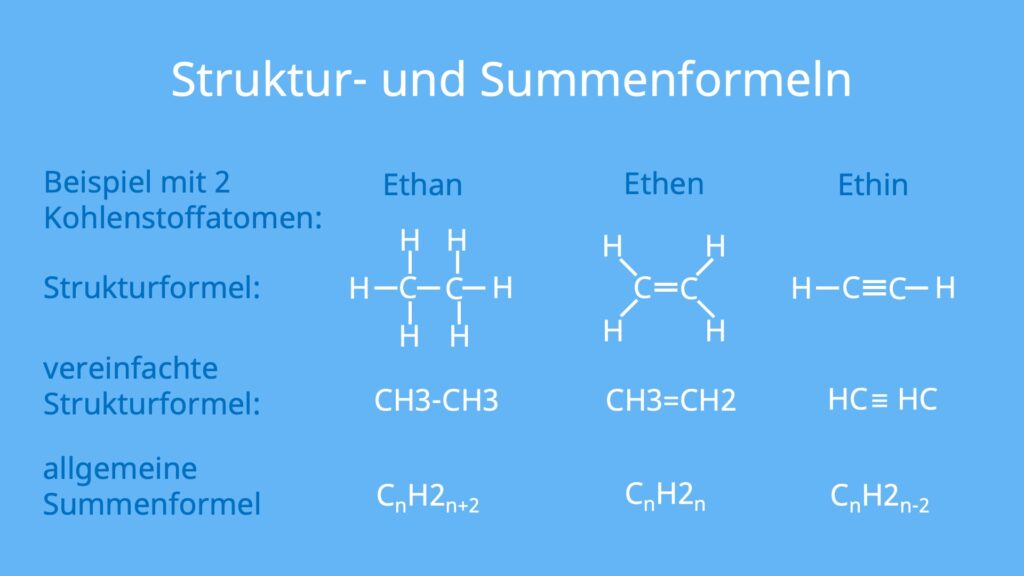
Auch in der Strukturformel unterscheiden sie sich von Alkanen und Alkinen. Wenn du ein Kohlenwasserstoff mit zwei Kohlenstoffatomen hast, würdest du als Alken CH2=CH2 (Ethen) schreiben, während du als Alkan CH3-CH3 (Ethan) und als Alkin HC≡CH (Ethin) schreibst.
Wie du an der Strukturformel von Ethan, Ethen und Ethin erkennst, haben Alkene und Alkine weniger Wasserstoffatome, weil sie durch die Doppel- bzw. Dreifachbindung weniger Wasserstoff binden können.
Nomenklatur Alkene
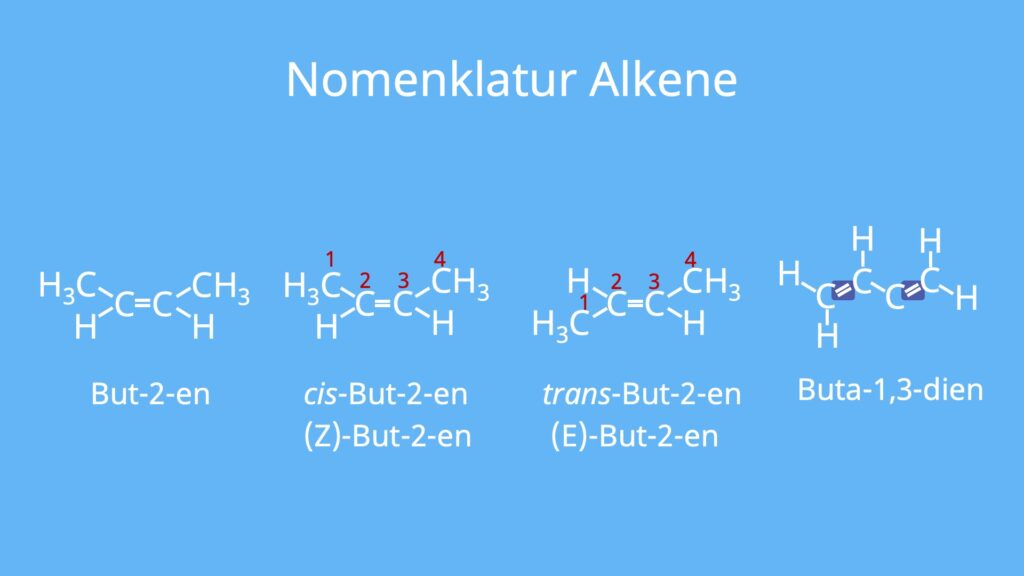
Alkene werden laut IUPAC Nomenklatur wie Alkane benannt, wobei sich das Suffix von -an zu -en ändert (teilweise auch -ylen). Je nachdem, an welchem Kohlenstoffatom die Doppelbindung liegt, wird eine Zahl entsprechend zur Position an den Namen zugefügt (z.B. 2-Buten oder But-2-en).
Die Zahl für die Position der Doppelbindung gibst du möglichst klein an, da es sich um eine funktionelle Gruppe handelt. Hast du zum Beispiel Penten mit der Strukturformel CH3-CH2-CH=CH-CH3, dann ist die Doppelbindung von links gezählt an dritter Stelle und von rechts gezählt an zweiter Stelle. Weil du die möglichst kleinste Zahl nimmst, handelt es sich hierbei also um 2-Penten.
Polyene
Liegen mehrere Doppelbindungen vor, sprichst du von Polyenen. Die Zahlen der Doppelbindungspositionen schreibst du dann direkt vor das -en und trennst sie mit einem Komma. Außerdem schreibst du vor das -en noch ein griechisches Zahlenwort passend zur Anzahl der Doppelbindungen, also di-, tri-, tetra- und so weiter. Hast du zum Beispiel ein Hexen mit der Strukturformel CH2=CH-CH-CH=CH2-CH3, heißt es Hexa-1,4-dien.
Cis-trans-Isomerie
Alkene können cis-trans-Isomere bilden, was mittlerweile auch (E,Z)-Isomerie genannt wird. Diese Art der Isomerie beschreibt, ob die Substituenten (Moleküle am Ende, z.B. -CH3) des Stoffes in die „entgegengesetzte“ (E) oder „zusammen“ (Z) in die gleiche Richtung zeigen. Die Bezeichnung cis- (Z-) oder trans- (E-) schreibst du an den Anfang von deinem Stoffnamen. Bei cis-But-2-en zeigen die -CH3-Enden beispielsweise in die gleiche Richtung.
Cycloalkene
Cycloalkene sind ringförmig angeordnet. Die Kohlenstoffatome bilden also einen Ring, wobei mindestens eine der Bindungen eine Doppelbindung ist. Dafür muss die Kette allerdings lang genug sein, weshalb das kleinste Cycloalken Cyclopropen (C3H4) ist. Die allgemeine Summenformel der Cycloalkene lautet CnH2n-2.
Homologe Reihe der Alkene
Durch die allgemeine Summenformel CnH2n bilden die Alkene eine homologe Reihe angefangen mit Ethen. Dabei wird in jedem Schritt der Reihe ein -CH2 hinzugefügt, also folgt auf Ethen das Propen, dann 1-Buten etc.
Die folgende Tabelle zeigt die homologe Reihe der unverzweigten Alkene mit bis zu 10 Kohlenstoffatomen und einer Doppelbindung am ersten Kohlenstoffatom:
| Name | IUPAC | Summenformel | vereinfachte Strukturformel |
|---|---|---|---|
| Ethylen | Ethen | C2H4 | CH2=CH2 |
| Propylen | Propen | C3H6 | CH2=CH-CH3 |
| 1-Buten | But-1-en | C4H8 | CH2=CH-CH2-CH3 |
| 1-Penten | Pent-1-en | C5H10 | CH2=CH-CH2-CH2-CH3 |
| 1-Hexen | Hex-1-en | C6H12 | CH2=CH-CH2-CH2-CH2-CH3 |
| 1-Hepten | Hept-1-en | C7H14 | CH2=CH-CH2-CH2-CH2-CH2-CH3 |
| 1-Octen | Oct-1-en | C8H16 | CH2=CH-CH2-CH2-CH2-CH2-CH2-CH3 |
| 1-Nonen | Non-1-en | C9H18 | CH2=CH-CH2-CH2-CH2-CH2-CH2-CH2-CH3 |
| 1-Decen | Dec-1-en | C10H20 | CH2=CH-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH3 |
Alkene Eigenschaften
Alkene besitzen Eigenschaften abhängig von ihrer Kohlenstoffatomzahl. Bei 2 bis 4 Kohlenstoffatomen sind sie unter Normalbedingungen gasförmig, bei 5 bis 15 flüssig und ab 16 Kohlenstoffatomen fest. Bis 12 Kohlenstoffatome sind sie sogar farblos.
Die Schmelz- und Siedepunkte erhöhen sich also mit zunehmender Länge der Alkenkette. Das liegt vor allem an den Van-der-Waals-Kräften , weil Alkene unpolare Moleküle sind und somit beispielsweise keine Wasserstoffbrückenbindungen ausbilden können. Die Van-der-Waals-Kräfte sind abhängig von der Oberfläche der Moleküle, welche bei größeren Alkenketten dementsprechend größer ist. Dadurch kommt es zu höheren Schmelz- und Siedepunkten.
Doppelbindungen sind kürzer als Einfachbindungen und reduzieren somit die Oberfläche. Mit nur einer Doppelbindung sind Schmelz- und Siedepunkt also höher als bei Polyenen, welche mehrere Doppelbindungen und somit eine kleinere Oberfläche besitzen.
Auch die Dichte nimmt mit der Anzahl der Kohlenstoffatome zu, wobei sie stets niedriger als die Dichte von Wasser ist. Da Alkene unpolar und somit lipophil (in Fett löslich) sind, lösen sie sich in unpolaren Lösungsmitteln, aber sind nur schwer wasserlöslich.
Im Vergleich zu Einfachbindungen sind Doppelbindungen deutlich instabiler und damit verantwortlich für eine hohe Reaktivität.
Alkene Reaktionen
Durch die hohe Reaktivität der Alkene, gehen sie vor allem Additionsreaktionen, genauer gesagt elektrophile Additionen ein. Dabei wird eine Doppelbindung aufgelöst, um zwei Einfachbindungen mit einem elektrophilen Stoff einzugehen. Am häufigsten passiert das mit Halogenen wie z.B. Brom Br2 (Halogenierung) oder mit Wasserstoff H2 (Hydrierung). Die Reaktion kann auch mit Halogenwasserstoffen HX (X ist ein beliebiges Halogen) oder in der Hydratisierung mit Wasser H2O auftreten.
Eine besondere Rolle spielt das Alken bei der Polymerisation . Dabei werden die Doppelbindungen angegriffen, um Polymere zu synthetisieren. Kurz gesagt werden die Doppelbindungen von Monomeren (wie z. B. Alken) durch Katalysatoren, Hitze oder Radikalen aufgelöst, um sich an weitere Monomere zu binden. So entsteht eine wachsende Kette an Monomeren, ein sogenanntes Polymer.
Alkene Herstellung und Nachweis
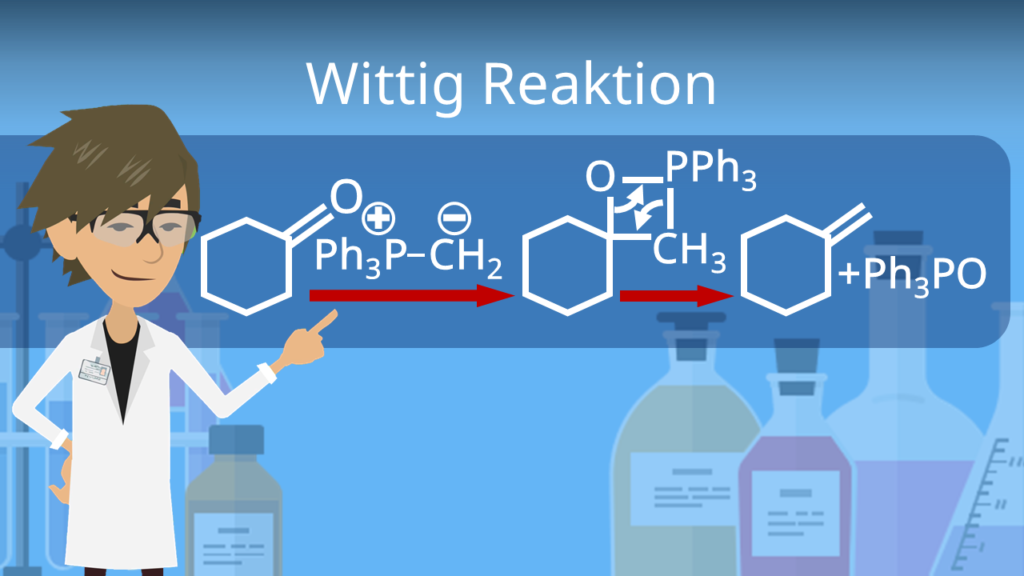
Alkene reagieren nicht nur zu anderen Stoffen, sondern können auch hergestellt werden. Das kann zum Beispiel durch die Wittig-Reaktion passieren, bei der ein Keton und ein Phosphor-Ylid zusammen zu Phosphinoxid und Alken reagieren.
Außerdem gibt es zwei Reaktionen, mit denen du das Vorhandensein von Alkenen nachweisen kannst, wie z.B.
- die Bromwasserprobe. Durch Hinzufügen von Alkenen zu braun gefärbtem Bromwasser, wird mit Brom eine Bindung aufgebaut, sodass sich das Wasser entfärbt. Diese Probe ist auch ein allgemeiner Nachweis für Mehrfachbindungen.
- die Baeyer-Probe. Hierbei wird zu dem Stoff, welchen du auf Alkene überprüfen möchtest, eine Kaliumpermanganat-Lösung KMnO4 hinzugegeben. Diese Lösung ist lila, aber färbt sich bei ungesättigten Kohlenwasserstoffen braun. Das liegt daran, dass die Doppelbindung des Alkens aufgelöst wird und dadurch ein Diol, Manganat(VI) und vor allem Braunstein entstehen.
Wittig-Reaktion
Jetzt weißt du das Wichtigste über Alkene von Nomenklatur bis Eigenschaften! Mithilfe der Wittig-Reaktion kannst du sie sogar herstellen! Möchtest du wissen, wie genau diese besondere Reaktion mit Phosphor-Ylid abläuft? Dann schau dir dazu unser Video an!