Du bist beim Lernen gerade über den Extinktionskoeffizient gestolpert und fragst dich, was dieser genau beschreibt und für was er eingesetzt wird. Kein Problem! In diesem Beitrag erklären wir dir, was der Extinktionskoeffizienten ist, wie du seine Einheit bestimmst und ihn berechnen kannst.
Du möchtest kurz ein wenig abschalten und den Extinktionskoeffizienten leicht verständlich erklärt bekommen? Dann schau unser Video dazu an.
Inhaltsübersicht
Extinktionskoeffizient einfach erklärt
Der Extinktionskoeffizient ist ein Maß, das angibt, wie stark sich elektromagnetische Strahlung beim Durchqueren eines Mediums abschwächt.
Prozesse die zur Abschwächung der Strahlung führen, sind zum Beispiel die Streuung und die Absorption. Der Extinktionskoeffizient tritt häufig in Bezug mit der Photometrie oder der UV/VIS-Spektroskopie auf.
Extinktionskoeffizient im Bereich Chemie
In der Chemie wird der Extinktionskoeffizient  auch molarer, dekadischer Extinktionskoeffizient oder molarer Absorptionskoeffizient genannt. Er beschreibt, wie viel Strahlung von einer bestimmten Substanz bei einer Weglänge von 1cm im Medium absorbiert wird. Berechnen lässt er sich mit Hilfe des Lambert Beerschen
Gesetzes
.
auch molarer, dekadischer Extinktionskoeffizient oder molarer Absorptionskoeffizient genannt. Er beschreibt, wie viel Strahlung von einer bestimmten Substanz bei einer Weglänge von 1cm im Medium absorbiert wird. Berechnen lässt er sich mit Hilfe des Lambert Beerschen
Gesetzes
.


Hierbei ist  die Extinktion, welche die Abschwächung der Intensität angibt. Sie ist definiert über den Logarithmus des Verhältnisses von der Intensität der einfallenden Strahlung
die Extinktion, welche die Abschwächung der Intensität angibt. Sie ist definiert über den Logarithmus des Verhältnisses von der Intensität der einfallenden Strahlung  und der Intensität der ausfallenden Strahlung
und der Intensität der ausfallenden Strahlung  . Die Intensität der einfallenden Strahlung wird dabei vor dem Durchqueren des Mediums gemessen und die Intensität der ausfallenden Strahlung nach dem Durchqueren des Mediums. Genaueres findest du in unserem Beitrag zum Lambert Beerschen Gesetz
. Des Weiteren repräsentiert die Variable
. Die Intensität der einfallenden Strahlung wird dabei vor dem Durchqueren des Mediums gemessen und die Intensität der ausfallenden Strahlung nach dem Durchqueren des Mediums. Genaueres findest du in unserem Beitrag zum Lambert Beerschen Gesetz
. Des Weiteren repräsentiert die Variable  in der oberen Formel die Stoffmengenkonzentration der Lösung und
in der oberen Formel die Stoffmengenkonzentration der Lösung und  die Schichtdichte der Küvette, in welcher sich die Substanz befindet.
die Schichtdichte der Küvette, in welcher sich die Substanz befindet.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Extinktionskoeffizient Einheit
Da die Stoffmengenkonzentration
 häufig in der Einheit
häufig in der Einheit ![Rendered by QuickLaTeX.com \left[ \frac{\mathrm{mol}}{\mathrm{l}}\right]](https://blog.assets.studyflix.de/wp-content/ql-cache/quicklatex.com-b7e746c79f3760c555b40321f792c61a_l3.png) angegeben wird und die Dicke der Küvette in
angegeben wird und die Dicke der Küvette in ![Rendered by QuickLaTeX.com \left[ \mathrm{cm}\right]](https://blog.assets.studyflix.de/wp-content/ql-cache/quicklatex.com-68e04cc205e0b3f890415834cb57e0d7_l3.png) , ergibt sich mit der dimensionslosen Extinktion nach der oberen Formel die Einheit des Extinktionskoeffizienten durch Liter pro Mol und Zentimeter
, ergibt sich mit der dimensionslosen Extinktion nach der oberen Formel die Einheit des Extinktionskoeffizienten durch Liter pro Mol und Zentimeter
![Rendered by QuickLaTeX.com \left[ \frac{\mathrm{l}}{\mathrm{mol} \cdot \mathrm{cm}} \right].](https://blog.assets.studyflix.de/wp-content/ql-cache/quicklatex.com-35b973d877bf120c76bc97f2a95e97db_l3.png)
Man kann die Stoffmengenkonzentration aber auch in der Einheit ![Rendered by QuickLaTeX.com \left[\frac{\mathrm{mol}}{\mathrm{cm}^3} \right]](https://blog.assets.studyflix.de/wp-content/ql-cache/quicklatex.com-4b08da6cc543d73b00b291eb170bba81_l3.png) angegeben. Damit ergibt sich für den Extinktionskoeffizienten dann die Einheit
angegeben. Damit ergibt sich für den Extinktionskoeffizienten dann die Einheit
![Rendered by QuickLaTeX.com \left[\frac{\mathrm{cm}^2}{\mathrm{mol}} \right].](https://blog.assets.studyflix.de/wp-content/ql-cache/quicklatex.com-31297b01f8d6462ae804fdec80bbef17_l3.png)
Extinktionskoeffizient im Bereich Optik
Auch im Bereich der Optik tritt der Extinktionskoeffizient  auf. Hier ist er über den Imaginärteil des Brechungsindexes
auf. Hier ist er über den Imaginärteil des Brechungsindexes 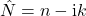 definiert.
definiert.  repräsentiert dabei den reellwertigen Brechungsindex. Der Brechungsindex ist allgemein eine dimensionslose Größe, welche das Verhältnis zwischen der Geschwindigkeit von elektromagnetischer Strahlung im Vakuum und der Geschwindigkeit im betrachteten Medium angibt. Betrachtet man eine Grenzfläche zweier verschiedener Medien, die einen unterschiedlichen Brechungsindex haben, dann wird Licht an der Grenzfläche gebrochen und reflektiert. Der Extinktionskoeffizient
repräsentiert dabei den reellwertigen Brechungsindex. Der Brechungsindex ist allgemein eine dimensionslose Größe, welche das Verhältnis zwischen der Geschwindigkeit von elektromagnetischer Strahlung im Vakuum und der Geschwindigkeit im betrachteten Medium angibt. Betrachtet man eine Grenzfläche zweier verschiedener Medien, die einen unterschiedlichen Brechungsindex haben, dann wird Licht an der Grenzfläche gebrochen und reflektiert. Der Extinktionskoeffizient  hängt dabei auch wieder von verschiedenen Faktoren, wie Wellenlänge der Strahlung, Temperatur, Kristallstruktur des Materials und noch mehr ab. Außerdem steht der Extinktionskoeffizient
hängt dabei auch wieder von verschiedenen Faktoren, wie Wellenlänge der Strahlung, Temperatur, Kristallstruktur des Materials und noch mehr ab. Außerdem steht der Extinktionskoeffizient  , der reelle Brechungsindex
, der reelle Brechungsindex  und der Absorptionskoeffizient
und der Absorptionskoeffizient  miteinander in Relation
miteinander in Relation

Extinktionskoeffizient berechnen
Im Folgenden wird gezeigt, was der imaginäre Brechungsindex physikalisch beschreibt und bewirkt. Dafür betrachten wir ein Beispiel mit ebenen Wellen. Eine ebene Welle kann durch folgende Gleichung beschrieben werden

Dabei steht  für die Frequenz und
für die Frequenz und  für die Zeit. Eine ebene Welle beschreibt eine senkrecht zur Ausbreitungsrichtung ausgedehnte Welle im dreidimensionalen Raum. Dabei ist die Wellenfront eine Ebene. Drückt man den Extinktionskoeffizienten mit der Phasengeschwindigkeit
für die Zeit. Eine ebene Welle beschreibt eine senkrecht zur Ausbreitungsrichtung ausgedehnte Welle im dreidimensionalen Raum. Dabei ist die Wellenfront eine Ebene. Drückt man den Extinktionskoeffizienten mit der Phasengeschwindigkeit  aus
aus

und setzt dies in die ebene Wellengleichung ein, erhält man




Der Term (*) beschreibt dabei die Amplitude der Welle in Abhängigkeit der Eindringtiefe  . Hieran kann man sehr gut erkennen, wenn der Extinktionskoeffizient positiv ist, also
. Hieran kann man sehr gut erkennen, wenn der Extinktionskoeffizient positiv ist, also  , dann nimmt die Amplitude der elektromagnetischen Welle beim Durchqueren des Mediums exponentiell ab.
, dann nimmt die Amplitude der elektromagnetischen Welle beim Durchqueren des Mediums exponentiell ab.
Extinktionskoeffizient berechnen Beispiel
Angenommen, man betrachtet eine Küvette mit einer Breite von 1cm, in der sich eine Substanz mit der Dichte 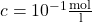 befindet. Erhält man anschließend durch Messung der Intensität des Lichts vor der Küvette und hinter der Küvette eine Extinktion von
befindet. Erhält man anschließend durch Messung der Intensität des Lichts vor der Küvette und hinter der Küvette eine Extinktion von  so lässt sich der Extinktionskoeffizient mit der obigen Formel berechnen durch
so lässt sich der Extinktionskoeffizient mit der obigen Formel berechnen durch


