Warum Eisberge schwimmen, kannst du mit der Anomalie des Wassers erklären. Was die Dichteanomalie des Wassers ist und was sie für eine Bedeutung in der Natur hat, erfährst du hier und im Video dazu!
Inhaltsübersicht
Was ist die Anomalie des Wassers?
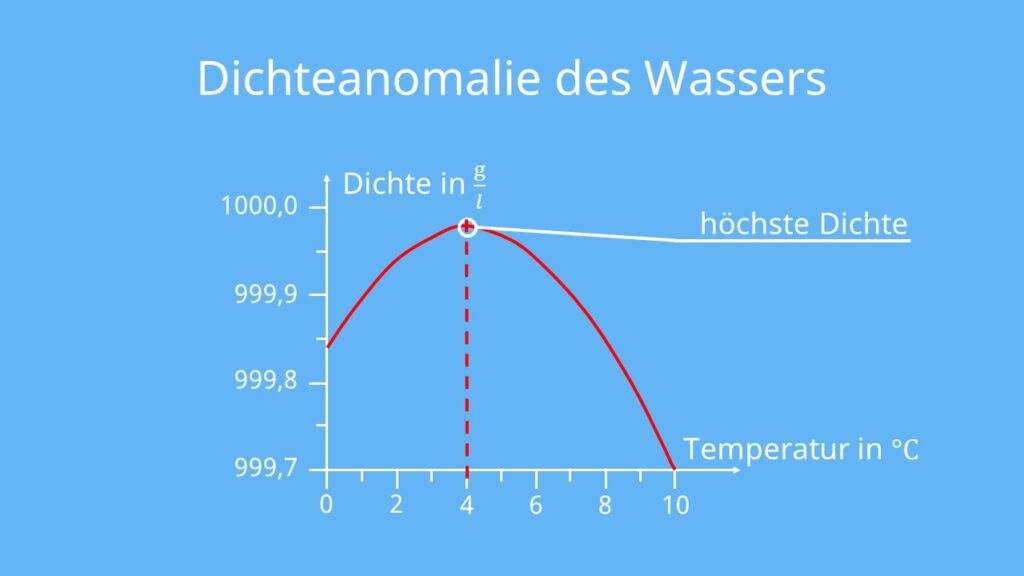
Die Anomalie des Wassers beschreibt, dass das Volumen von Wasser beim Abkühlen nur bis zu einer Temperatur von 4°C sinkt und dort sein Minimum erreicht. Wird es ab dieser Temperatur weiter erhitzt oder abgekühlt, nimmt das Volumen zu. Ein höheres Volumen führt zu einer geringeren Dichte. Deshalb wird es auch Dichteanomalie des Wassers genannt.
Durch diese Wasser Anomalie schwimmt das Eis eines zugefrorenen Sees wegen seiner geringeren Dichte an der Oberfläche. Dadurch bleibt das Wasser unterhalb der Eisschicht ausreichend warm, sodass die Fische im Winter überleben.
Gut zu wissen: Normalerweise nimmt die Dichte bei sinkender Temperatur von Flüssigkeiten kontinuierlich zu. Wasser stellt somit die einzige Ausnahme dar.
Anomalie des Wassers — Erklärung
Für die Erklärung der Anomalie ist es wichtig zu wissen, dass Wasser aus kleinen Gruppen von Molekülen besteht. Diese werden von Wasserstoffbrückenbindungen zusammengehalten, welche für die Anomalie verantwortlich sind.
Was bei einer Temperaturänderung mit diesen Bindungen passiert, lässt sich bei einem Blick auf die kleinen Wasserteilchen erkennen:
-
Warmes Wasser (über 4° Celsius): Wenn die Temperatur von Wasser über 4° Celsius steigt, bewegen sich die Moleküle schneller. Als Folge werden die Wasserstoffbrückenbindungen schwächer. Dadurch dehnt sich das Wasser aus, weshalb die Dichte abnimmt.
-
Kaltes Wasser (unter 4° Celsius): Beim Abkühlen auf unter 4° Celsius bewegen sich die Moleküle langsamer. So bilden sich größere Gruppen von Wassermolekülen in Form von weitmaschigen Kristallen. Zwischen den Teilchen ist also viel Platz. Das höhere Volumen führt dazu, dass sich die Dichte verringert. Das kann bei Eiskristallen gut beobachtet werden.
Zusammengefasst: Das Verhalten der Wasserstoffbrückenbindungen sorgt für die Dichteanomalie des Wassers.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Anomalie des Wassers in der Natur
In der Natur spielt die Anomalie des Wassers eine lebenswichtige Rolle für das Überleben von Tieren und Pflanzen bei kalten Wintertemperaturen.
Ein bekanntes Beispiel dafür ist ein See bei verschiedenen Jahreszeiten:
Sommer: Im Sommer erwärmt die Sonne die obere Schicht des Sees. Schichten mit einer höheren Dichte sinken nach unten und Schichten mit geringerer Dichte liegen oben. Deshalb bleibt das leichtere, wärmere Wasser oben und die kühleren, schweren Wasser-Schichten unten im See. Das Wasser nimmt also keine einheitliche Temperatur an.
Herbst: Im Herbst ist die Sonnenstrahlung nicht mehr so stark und die Luft kühler. Deshalb kühlt sich auch das Wasser nach und nach ab. Wasserströmungen sorgen nun dafür, dass es einen Temperaturausgleich gibt.
Winter: Im Winter verringert sich die Temperatur des Wassers und es entstehen verschiedene Schichten. Bei 4° Celsius erreicht Wasser seine größte Dichte. Das bis 4°C warme Wasser sinkt daher nach unten. Dahingegen befindet sich das abgekühlte See-Wasser eher an der Oberfläche.
Bei 0°C gefriert das Wasser schließlich. Da Eis die geringste Dichte hat, schwimmt es auf der Wasseroberfläche. Die gefrorene Schicht schützt die flüssigen Schichten darunter vor dem Gefrieren. Ist das Gewässer ausreichend tief, entsteht in der Tiefe ein ca. 4° Celsius warmer Bereich. Darin überleben die Bewohner des Sees.
Frühling: Im Frühjahr sind die Sonnenstrahlen intensiver. Dadurch wird das Wasser wieder wärmer. Die Wasserschichten durchmischen sich und es kommt zum Temperaturausgleich.
Anomalie des Wassers im Alltag
Auch im Alltag hat die Dichteanomalie des Wassers eine Bedeutung. Gefrierendes Wasser hat nämlich eine Sprengwirkung, da das Volumen wegen der Wasser Anomalie ab unter 0°C plötzlich viel größer wird.
Die Sprengwirkung macht sich auch in anderen Bereichen des Alltags bemerkbar:
- Frei liegende Wasserrohre können im Winter auseinandersprengen.
- Steinbrocken werden von Felsen abgespalten, wenn Wasser in die Risse der Felswände gelangt und im Winter friert.
Achtung: Du solltest die Sprengwirkung beachten, wenn du eine Wasserflasche in das Gefrierfach stellst! Gefriert das Wasser darin, so sprengt die plötzliche Ausdehnung die Flasche gewaltsam auf.
Anomalie des Wassers — Temperatur
Die Temperatur hat einen Einfluss auf die Dichte des Wassers, wobei bei 4°C ein Dichte-Maximum erreicht wird. Links und rechts von diesem Hochpunkt nimmt die Dichte kontinuierlich ab.
Wenn du die Masse der Flüssigkeit durch das Volumen teilst, ergibt das die Dichte:
![Rendered by QuickLaTeX.com \[ \rho = \frac{m}{V}\]](https://blog.assets.studyflix.de/wp-content/ql-cache/quicklatex.com-497fe1fbc314e65b232f6842d5a3a83c_l3.png)
Es besteht also ein unmittelbarer Zusammenhang zwischen dem Volumen und der Dichte des Wassers:
- Mehr Volumen ⇒ Niedrigere Dichte
- Weniger Volumen ⇒ Höhere Dichte
Dieser Zusammenhang gilt aber nur, wenn die Masse des Wassers bei der Veränderung des Volumens gleich bleibt.
Gut zu wissen: Die Dichte von Wasser beträgt bei 4°C ungefähr 1 g/cm3.
Dichte Wasser
Jetzt weißt du, wie die Dichte von Wasser sich bei unterschiedlicher Temperatur verhält. Wie du mithilfe der Wasserdichte und einfachen Haushaltsmitteln die Dichte von anderen Flüssigkeiten herausfinden kannst, erfährst du in diesem Video dazu!