Exotherme und Endotherme Reaktion
In diesem Beitrag wiederholen wir noch einmal die Unterschiede und wesentlichen Merkmale von exo- beziehungsweise endothermen Reaktionen.
Inhaltsübersicht
Exotherm und Endotherm
Als exotherm gilt eine Reaktion, wenn die Produkte eine niedrigere Enthalpie als die Edukte aufweisen. Mehr über Enthalpie erfährst du in unseren Videos zur Definition der Enthalpie , Reaktionsenthalpie und zur Freien Enthalpie .
Endotherm ist dementsprechend das genaue Gegenteil zu exotherm. Hier spricht man von einer Zunahme an Enthalpie. Was das genau bedeutet, schauen wir uns jetzt anhand eines einfachen Beispiels an.
Endothermen Reaktion – Beispiel
Bestimmt hast du schon mal eine Brausetablette in Wasser aufgelöst. Beim Auflösen des Brausepulvers, einem Gemisch aus Zitronensäure + Natriumhydrogencarbonat, wird die Lösungsenergie für die Reaktion dem Wasser entzogen. Das Wasser kühlt sich bei diesem Vorgang etwas ab.
Folglich wird Energie in Form von Wärme aus der Umgebung aufgenommen und die Reaktion ist damit endotherm.
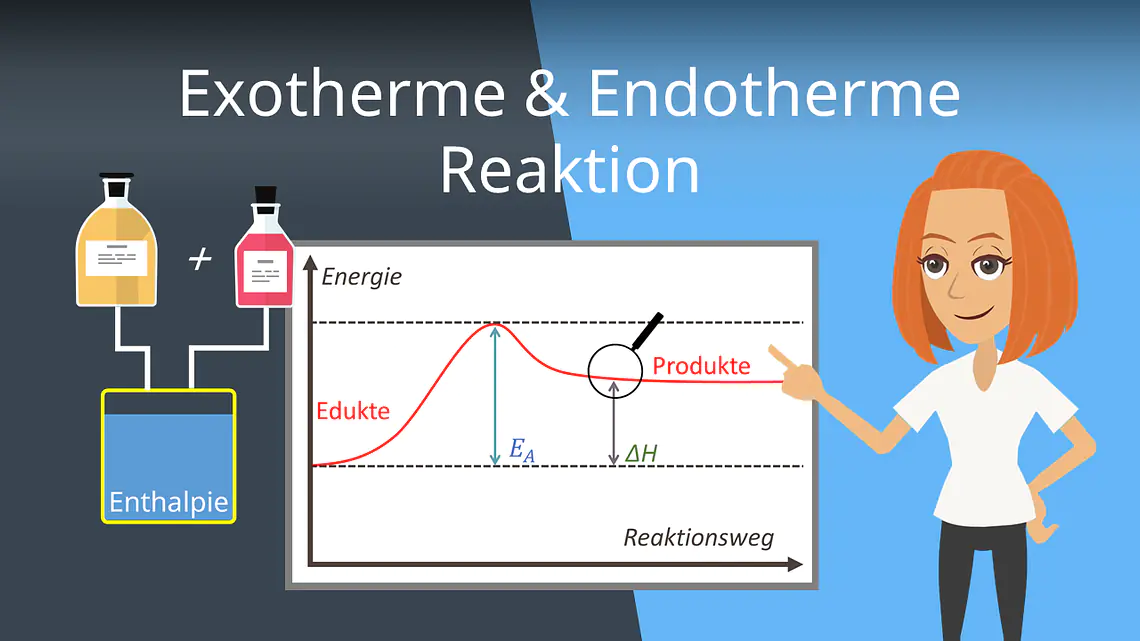
Graphisch lässt sich die endotherme Reaktion wie folgt darstellen:
Auf der Y-Achse des Graphen tragen wir die Energie ab, während die X-Achse den Reaktionsweg beschreibt.
Zunächst haben wir die Ausgangsstoffe Zitronensäure und Natriumhydrogencarbonat mit einer gewissen Energie. Diesen Ausgangsstoffen führen wir nun Energie zu – besser gesagt, sie entziehen die Energie der Umgebung, wodurch das Energielevel weiter ansteigt. Sobald dann ein bestimmter Punkt erreicht ist, genügt die Energie, um die Reaktion ablaufen zu lassen. Am Ende der Reaktion haben dann die Endstoffe mehr Energie als die Ausgangsstoffe, da die Energie aus der Umgebung aufgenommen wurde.
Aktivierungsenergie und Exotherme Reaktion – Beispiel
Wie bereits erwähnt, ist es bei einer exothermen Reaktion genau umgekehrt. Wir schauen uns zur Verdeutlichung eine Verbrennungsreaktion an.
Wenn du mit deinen Freunden am Lagerfeuer sitzt, findet dort eine exotherme Reaktion statt.
Der Ausgangsstoff, in diesem Fall Holz, hat am Anfang wieder ein gewisses Energielevel. Holz allein brennt aber noch nicht von selbst. Wir müssen dem System wieder etwas Energie zuführen, damit die Reaktion stattfinden kann, die sogenannte Aktivierungsenergie. Das ist zum Beispiel die Energie, die du zuführst, wenn du das Lagerfeuer anzündest.
Wenn du dem System ausreichend Energie zugeführt hast, fängt das Holz an zu brennen und die Reaktion läuft von selbst ab.
Bei der Reaktion wird Energie in Form von Wärme freigesetzt. Das merkst du ganz einfach daran, dass sich die Luft um das Lagerfeuer zu erwärmen beginnt. Folglich wird Energie an die Umgebung abgegeben und die Reaktion ist damit exotherm.
Nun weißt du, wie du Reaktionen thermisch einordnen kannst. Viel Spaß und bis bald!