Was es mit dem Elektron auf sich hat, was das Besondere daran ist und warum es eines der wichtigsten Elementarteilchen ist erfährst du hier und im Video !
Inhaltsübersicht
Elektron einfach erklärt
In fast allen physikalischen Effekten spielen Elektronen eine bedeutende Rolle. Da Elektronen Ladung tragen, erzeugen sie auch ein elektrisches Feld . Setzt du das Elektron in Bewegung, erhältst du dazu ein magnetisches Feld . Durchdringt ein Elektron ein anderes externes elektrisches Feld, wird dessen Bahn aufgrund der Lorentzkraft verändert.
Die in einem Atom gebunden Elektronen, bilden dessen Elektronenhülle . In der Chemie sind vor allem diese von Bedeutung.
Das Elektron ( ) ist ein subatomares Teilchen mit negativer Ladung. Seine Ladung wird auch als Elementarladung bezeichnet. Sie werden als Elementarteilchen bezeichnet, da unbekannt ist ob sie aus anderen Komponenten zusammengesetzt sind. Wie es allen Elementarteilchen gemein ist, haben Elektronen einen Wellen- und einen Teilchencharakter. Das heißt sie können mit anderen Teilchen kollidieren aber auch gebeugt werden wie Licht.
) ist ein subatomares Teilchen mit negativer Ladung. Seine Ladung wird auch als Elementarladung bezeichnet. Sie werden als Elementarteilchen bezeichnet, da unbekannt ist ob sie aus anderen Komponenten zusammengesetzt sind. Wie es allen Elementarteilchen gemein ist, haben Elektronen einen Wellen- und einen Teilchencharakter. Das heißt sie können mit anderen Teilchen kollidieren aber auch gebeugt werden wie Licht.
Merke
Das Elektron ist ein negativ geladenes Elementarteilchen. Seine Ladung wird auch als Elementarladung bezeichnet.
Was ist ein Elektron?
Das Elektron gehört zur Teilchenfamilie der Leptonen. Es gibt mehrere verschiedene Familien von Teilchen, die im Standardmodell der Teilchenphysik aufgeführt sind. Schau dazu am besten noch das Video an.
Leptonen sind, nach bisherigem Wissensstand, Elementarteilchen. Verglichen mit anderen Leptonen, hat das Elektron die geringste Masse der ladungstragenden Leptonen. Es gehört zur ersten Generation der Leptonen. Die zweite und dritte Generation bilden das Myon und das Tauon. Diese beiden Teilchen haben identische Ladungen und Spin wie das Elektron, unterscheiden sich aber in ihrer höheren Masse davon. Von anderen fundamentalen Teilchen, wie den Quarks, unterscheiden sich Leptonen aufgrund der Abwesenheit der starken Wechselwirkung. Alle Leptonen gehören zur Familie der Fermionen, weswegen das Elektron einen Spin von  hat.
hat.
| Ladung | – 1 e C C |
| Ruhemasse |
 kg kg u u |
| Ruheenergie |
 MeV MeV J J |
| Compton-Wellenlänge |
 m m |
| magnetisches Moment |
 J/T J/T |
| g-Faktor |  |
| Spin | 1/2 |
| mittlere Lebensdauer | >  a a |
| Wechselwirkung | schwach elektromagnetisch Gravitation |
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Eigenschaften Elektron
Das Elektron wird neben dem Spin aber noch durch weitere Eigenschaften charakterisiert. seine sogenannte invariante Masse beträgt in etwa 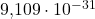 Kilogramm oder auch
Kilogramm oder auch  atomare Masseneinheiten.
Aufgrund der Äquivalenz von Masse und Energie nach dem Relativitätsprinzip
ergibt sich daraus eine Ruheenergie von 0,511 MeV (Mega-Elektronen-Volt). Das Verhältnis der Masse eines Protons zu der eines Elektrons beträgt 1836. Zudem trägt es eine Ladung von
atomare Masseneinheiten.
Aufgrund der Äquivalenz von Masse und Energie nach dem Relativitätsprinzip
ergibt sich daraus eine Ruheenergie von 0,511 MeV (Mega-Elektronen-Volt). Das Verhältnis der Masse eines Protons zu der eines Elektrons beträgt 1836. Zudem trägt es eine Ladung von  Coulomb. Das Elektron hat einen intrinsisches Drehmoment, beziehungsweise einen Spin, von 1/2. Dazu hat es ein intrinsisches magnetisches Moment entlang der Spin Achse. Dieses beträgt in etwa
Coulomb. Das Elektron hat einen intrinsisches Drehmoment, beziehungsweise einen Spin, von 1/2. Dazu hat es ein intrinsisches magnetisches Moment entlang der Spin Achse. Dieses beträgt in etwa 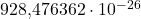 Joules pro Tesla.
Joules pro Tesla.
Atome und Moleküle
Elektronen sind durch die anziehende Coulomb Kraft an Atomkerne gebunden. Eine solche Zusammensetzung aus Atomkern und einem oder mehr Elektronen bezeichnet man als Atom. Unterscheidet sich die Zahl der Elektronen von der Kernladung handelt es sich um ein Ion. Die Wellennatur der gebunden Elektronen wird über die Atom Orbitale beschrieben. Jedes dieser Orbitale hat eine Reihe von Quantenzahlen wie Energie und Drehmoment. Zudem kann ein Atom nur eine diskrete Zahl von Orbitalen haben. Aufgrund des Pauli–Prinzips können maximal zwei Elektronen in einem Orbital sein, deren Spin verschiedene Vorzeichen haben.
Die chemische Bindung zwischen Atomen geschieht durch elektromagnetische Wechselwirkungen, welche mit der Quantenphysik beschrieben werden. Die stärksten Bindungen werden durch das Teilen oder Transferieren von Elektronen geschaffen. Das ermöglicht die Bildung von Molekülen . In Molekülen bewegen sich Elektron ähnlich wie in Atomen und belegen molekulare Orbitale. Ein grundlegender Unterschied ist jedoch die Ausbildung von Elektronenpaaren mit unterschiedlichen Spins. Dadurch belegen mehrere Elektronen ein Orbital ohne das Pauli–Prinzip zu verletzen.
Elektron Masse
Die Masse des Elektrons wurde hier als invariante Masse bezeichnet. Mit diesem Begriff wird der Anteil der Gesamtmasse eines Objekts beschrieben, der unabhängig vom Gesamtimpuls des umgebenden Systems ist. Das heißt es ist ein charakteristischer Wert, gebildet aus der Gesamtenergie und dem Gesamtimpuls, welcher in allen Bezugssystemen gleich bleibt. Somit ist die invariante Masse invariant unter Lorentztransformation.
Elektron Ladung
Das Elektron hat eine Ladung von  . Das
. Das  steht dabei für Elementarladung. Dies ist die kleinste frei existierende Ladungsmenge. Die Ladung freier Teilchen ist entweder Null oder ein ganzzahliges vielfaches von
steht dabei für Elementarladung. Dies ist die kleinste frei existierende Ladungsmenge. Die Ladung freier Teilchen ist entweder Null oder ein ganzzahliges vielfaches von  . Daher besitzen Elektronen und Myonen Ladungen von
. Daher besitzen Elektronen und Myonen Ladungen von  und Teilchen wie Protonen
und Teilchen wie Protonen  .
.
Elektron Energie
Die Energie des Elektrons berechnet sich aus der Äquivalenz von Masse und Energie. Diese kennst du als die Formel aus der Relativitätstheorie  .
.  steht für Energie,
steht für Energie,  für Masse und
für Masse und  für die Lichtgeschwindigkeit.
für die Lichtgeschwindigkeit.
Elektron Leitfähigkeit
Die Leitfähigkeit eines Mediums hängt davon ab, wie frei sich Elektronen in diesem Medium bewegen können. In einem Leiter sind die äußeren Elektronen der Atome weitestgehend frei und können sich ähnlich wie eine Flüssigkeit zwischen den Atomen bewegen. In einem Isolator sind die Elektronen ortsfest an ihre Atome gebunden, was ihre Bewegungsfreiheit stark einschränkt. Diese Elektronen können nur durch Energiezufuhr gelöst werden (z.B. indem die Temperatur erhöht wird). Eine besondere Form Stellen Halbleiter dar. Diese haben zwei Energiebänder, das Valenz– und das Leitungsband. Abhängig von der Dotierung und Temperatur des Halbleiters, sind diese als Leiter oder Isolatoren verwendbar.
Willst du mehr zum Halbleiter erfahren schau auf jeden Fall noch unser Video zu dem Thema an.
Elektronen, Protonen, Neutronen
Für dich von Bedeutung ist es, den Unterschied zwischen den drei wichtigsten Nukleonen zu kennen.
Zunächst das Elektron. Hierbei handelt es sich um ein negativ geladenes Elementarteilchen mit Spin 1/2 und sehr geringer Masse. Elektronen bilden die Atomhülle um einen Atomkern. Die Anzahl der darin enthaltenen Elektronen ist bei neutralen Atomen gleich der Anzahl an Protonen im Kern.
Das Proton ist kein Elementarteilchen. Es ist aus drei Quarks zusammengesetzt und hat eine positive Ladung. Zusammen mit Neutronen bilden Protonen den Atomkern. Zusammen bezeichnet man diese dann als Nuklid .
Das Neutron besteht auch aus drei Quarks. Deren Zusammensetzung führt jedoch dazu, dass das Neutron ungeladen, also neutral ist. Neutronen sind wichtig für die Stabilität eines Atomkerns.
Wie das Elektron haben auch Protonen und Neutronen einen Spin von 1/2. Somit gehören auch sie zur Familie der Fermionen.
