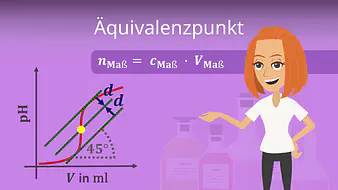Mit der Titration kannst du leicht bestimmen, wie viel einer chemischen Substanz in einer Flüssigkeit vorhanden ist. Somit kannst du zum Beispiel den Säure- und Basegehalt der Flüssigkeit bestimmen. Alles weitere Interessante, findest du hier! Möchtest du den ganzen Inhalt lieber audiovisuell aufbereitet sehen, dann schaue dir auf jeden Fall unser Video an!
Inhaltsübersicht
Titration einfach erklärt
Bei der Titration handelt es sich um ein chemisches Analyseverfahren, bei welcher du die Konzentration eines der Bestandteile einer Probelösung bestimmen kannst. Dafür musst du aber schon vorher wissen, um welche Substanz es sich dabei handelt. Man kann also nur die Konzentration eines Bestandteils, nicht aber die Bestandteile einer Lösung an sich, bestimmen. Am Anfang steht deine Probelösung, bei der du die Konzentration einer der Bestandteile bestimmen willst. Um dies zu erreichen benötigst du eine Maßlösung. Von dieser kennst du bereits die Bestandteile und deren Konzentration. Diese Maßlösung setzt die zu bestimmende Substanz chemisch um. Du gibst solange weiter die Maßlösung hinzu bis du den Äquivalenzpunkt erreicht hast. An diesem Punkt wurde die Probelösung komplett umgesetzt und es herrscht so Stoffmengengleichheit zwischen Probe- und Analysemoleküle. Was genau du zum Äquivalenzpunkt wissen musst, erfährst du in unserem Artikel und unserem Video dazu! Anschließend kann man über das verbrauchte Volumen an Maßlösung und die bekannte Reaktionsgleichung bestimmen, in welcher Konzentration der Stoff in der Probelösung vorliegt.
Titration Reaktionsarten
Die Art der Reaktion, mit der man die zu bestimmende Substanz umsetzt, ist bei der Titration entscheidend. Im Folgenden bekommst du einen kurzen Überblick über die verschiedenen Arten, die sich in der Titration etabliert haben.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Säure-Base Titration
Die wahrscheinlich bekannteste Art der Titration ist die Säure-Base Titration. Wie der Name es dir schon verrät, setzt man hierbei die Substanz in einer Bronsted Säure-Base Reaktion um. Dafür muss die zu analysierende Substanz natürlich auch eine Säure oder eine Base sein. Die Menge an umgesetzter Substanz kann man dabei anhand des pH-Werts verfolgen. Durch Verwendung eines Indikators mit passendem Umschlagspunkt kann man außerdem bestimmen, wann die gesamte Menge der Säure/Base der Probelösung abreagiert hat. In der Titrationskurve ergibt sich an dieser Stelle ein Wendepunkt, der Äquivalenzpunkt. Möchtest mehr zur Säure-Base Titration erfahren, dann schaue dir unbedingt unser Video dazu an!
Fällungstitration und Argentometrie
In der Fällungstitration dagegen wird die zu analysierende Substanz durch eine Reaktion in eine unlösliche Verbindung umgewandelt, die ausfällt. Sobald die Konzentration dieses unlöslichen Stoffs sein geringes Löslichkeitsprodukt überschreitet, fällt dieser als Feststoff aus. Dieser Punkt des Ausfallens oftmals farbiger Feststoffe markiert dann das Erreichen des Äquivalenzpunktes. An diesem lässt sich über das Löslichkeitsprodukt die Konzentration der gesuchten Substanz bestimmen. Ein häufiger Vertreter dieser Art der Titration ist die Argentometrie, bei der Konzentration von Halogenid-Ionen durch Bildung von Silberhalogeniden bestimmt werden kann.
Redox Titration
Diese Art von Titration bedient sich der Redox-Reaktionen, um die zu analysierende Substanz umzusetzen. Auch hier ist das Ziel, eine komplette Umsetzung der Probelösung durch die Maßlösung. Häufig verwendete Maßlösungen sind Permanganat- und Iodlösungen aufgrund ihrer sehr starken Färbung. Da beim Erreichen des Äquivalenzpunktes kein Reaktionspartner mehr zur Verfügung steht, färbt sich auch die Probelösung. Dies kann man dann als Erreichen des Äquivalenzpunktes erkennen. Daher braucht man bei Anwendung dieser Maßlösungen keinen zusätzlichen Indikator.
Komplexometrie
Diese, auch als Chelatometrie bekannte Titrationsmethode wird eingesetzt, um den Gehalt von Metallionen in einer Lösung zu bestimmen. Dabei wird der Probelösung zuerst eine Indikatorlösung mit Komplexen hinzu gegeben. Diese Komplexe binden sich an die in der Lösung vorhandenen Metallionen und erzeugen eine bestimmte Färbung der Lösung. Anschließend wird mit einer Maßlösung titriert. Diese Maßlösung enthält auch wieder Komplexe, jedoch handelt es sich hierbei um mehrzähnige Liganden, wie zum Beispiel EDTA, ein 6-zähniger Ligand. Durch diese höhere Zahl an möglichen Koordinationsstellen (Chelat-Effekt) verdrängen die Moleküle der Maßlösung die Indikatormoleküle aus der Koordinationsumgebung der Metallionen. Ohne ein an sich gebundenes Metallionen weisen die Indikatormoleküle eine andere Färbung auf. Sind alle Indikatormoleküle verdrängt ergibt sich also ein Farbumschlag der Probelösung. Ein Nachteil dieser komplexometrischen Titration ist, dass viele Maßlösungen nur wenig unterscheiden können, an welches Metall-Ion sie sich binden. Daher ist diese Methode nur wenig selektiv.
Titration Berechnung und Auswertung
Die Auswertung aller Ergebnisse der Titration beruht auf der Erkennung des Äquivalenzpunktes und Analyse der Titrationskurve. An diesem Punkt besteht eine Gleichheit zwischen der umgesetzten Stoffmenge der Maßlösung  und die der Probelösung
und die der Probelösung  . Die umgesetzte Stoffmenge der Probelösung entspricht der gesamten in der Probelösung enthaltenen Menge.
. Die umgesetzte Stoffmenge der Probelösung entspricht der gesamten in der Probelösung enthaltenen Menge.

Die umgesetzte Stoffmenge der Maßlösung kennst du, weil du das zugegebene Volumen  gemessen hast und auch die Konzentration
gemessen hast und auch die Konzentration  der Maßlösung kennst.
der Maßlösung kennst.

Da du auch das Gesamtvolumen der Probelösung  messen kannst, erhältst du dann folgende Gleichung für die Konzentration der Probelösung
messen kannst, erhältst du dann folgende Gleichung für die Konzentration der Probelösung  :
:

Titration Arten
Neben den Reaktionstypen kannst du auch noch die Titration unterscheiden in direkte und indirekte Titration unterscheiden.
Direkte Titration
Die direkte Titration läuft so ab, wie bisher beschrieben. Du verwendest eine Maßlösung, deren Reagenz direkt den gewünschten Bestandteil chemisch umsetzt.
Indirekte Titration
Die indirekte Titration geht dagegen einen etwas umständlicheren Weg. Dabei setzt man zuerst die zu analysierende Substanz in der Probelösung chemisch um. Dann fügt man ein festes Volumen an Maßlösung hinzu. Dieses setzt die Substanz erneut chemisch um. Der Unterschied zur direkten Titration besteht aber darin, dass du immer mehr Maßlösung hinzusetzt als Probelösung vorhanden ist. Dadurch bleibt ein Rest an nicht umgesetzter Maßlösung über. Von diesem Rest wiederum wird in einer direkten Titration die Stoffmenge bestimmt. Kennt man die jeweilige Stoffmenge, kann man auch auf die Konzentration der Probelösung schließen. Wegen der erneuten Titration der Maßlösung wird das Verfahren auch als Rücktitration bezeichnet.
Unterscheidung nach Endpunktbestimmung
Wichtiger Teil einer Titration ist es immer, möglichst genau anhand der Titrationskurve bestimmen zu können, wann die Probelösung komplett von der Maßlösung umgesetzt worden ist. Daher haben sich über die Zeit mehrere Methoden zur Endpunktbestimmung durchgesetzt.
Endpunktbestimmung mit Indikatorlösungen
Die am einfachsten umsetzbare Methode zur Endpunktbestimmung ist die Verwendung von Indikatorlösungen. Diese erzeugen immer dann einen Farbumschlag der Probelösung, wenn die komplette enthaltene Stoffmenge der zu bestimmenden Substanz umgesetzt worden ist. Ein sehr bekannter Indikator in der Säure-Base Titration ist das Phenolphthalein. Dieser Indikator ist bei einem pH-Wert von 0-8,2 farblos. Erst bei einem Überschreiten des pH-Werts von 8,2 schlägt die Farbe des Phenolphthalein in ein grelles Pink um. Durch den Umschlagspunkt im basischen Bereich eignet sich dieser Indikator für die Titration von schwachen Säuren. Weiterhin kann auch das Reaktionsprodukt aus Maß- und Probelösung selbst als Indikator dienen. Dies wird bei der Fällungstitration ausgenutzt, bei der das Ausfallen eines Feststoffs als Endpunkt gewertet wird.
Endpunktbestimmung bei der Potentiometrie
Eine weitere, im Vergleich zum Farbumschlag, exaktere Bestimmung des Endpunkts kann auch über die Potentiometrie erfolgen. In diesem Fall nutzt man aus, dass das elektrochemische Potential einer Lösung nach der Nernst-Gleichung konzentrationsabhängig ist. Um dieses zu messen, taucht man eine Messelektrode in die Probelösung und misst die Spannung zu einer Bezugselektrode, die auf konstantem Potential liegt. Wird durch das Zugeben der Maßlösung die Konzentration der Probelösung schrittweise reduziert , verändert sich auch die gemessene Spannung. Bis zum Erreichen des Endpunktes ändert sich die Spannung nur geringfügig, erst beim Überschreiten kommt es zu einer schlagartigen Änderung. Dadurch kann man den Endpunkt leicht erkennen. Du möchtest noch weitere Information zur Potentiometrie? Dann schau unbedingt in unserem Artikel und unserem Video zur Potentiometrie vorbei!
Endpunktbestimmung bei der Konduktometrie
Die letzte Art den Endpunkt zu bestimmen ist die Konduktometrie. Diese versucht anhand der elektrolytischen Leitfähigkeit den Endpunkt zu erkennen. Um diese messen zu können, werden zwei inerte Messelektroden in die Probelösung getaucht. Anschließend fließt über Anlegen einer Wechselspannung ein Wechselstrom über die Elektroden durch die Probelösung. Daraus lässt sich der Widerstand bzw. die elektrische Leitfähigkeit bestimmen. Eine Voraussetzung dafür ist, dass die zu messende Substanz in der Lösung als Ion vorliegt, das den Wechselstrom tatsächlich über Diffusion in der Lösung übertragen kann. Bei Zugabe der Maßlösung werden diese Ionen dann neutralisiert, wie zum Beispiel beim Hinzugeben einer Base zu einer Säure die Oxonium- und Hydroxid-Ionen neutralisiert werden. Dadurch sinkt dann auch schrittweise die Leitfähigkeit, weil weniger Ladungsträger zur Verfügung stehen. Erst ab Erreichen des Endpunkts nimmt die Leitfähigkeit wieder stark zu, weil dann die weiterhin hinzu gegebenen Ionen aus der Maßlösung nicht neutralisiert werden und damit die Konzentration an Ladungsträgern wieder zunimmt. Man kann den Endpunkt also anhand eines Knicks im in der Titrationskurve erkennen.
Titration — häufigste Fragen
(ausklappen)
Titration — häufigste Fragen
(ausklappen)-
Wie wähle ich den passenden Indikator für eine Säure-Base-Titration aus?Du wählst den Indikator so, dass sein Umschlagsbereich im steilen pH-Sprung um den Äquivalenzpunkt liegt. Das klappt gut, weil dort schon kleine Volumenänderungen den pH stark verändern. Beispiel: Bei starker Säure gegen starke Base passt Bromthymolblau, bei schwacher Säure gegen starke Base oft Phenolphthalein.
-
Wie berücksichtige ich die Stöchiometrie, wenn Maßlösung und Probelösung nicht im 1:1-Verhältnis reagieren?Du musst die Stoffmengen über die Reaktionsgleichung verknüpfen, statt einfach
 zu setzen. Konkret gilt
zu setzen. Konkret gilt  , wobei
, wobei  die stöchiometrischen Koeffizienten sind. Beispiel: Bei
die stöchiometrischen Koeffizienten sind. Beispiel: Bei  entspricht 1 mol Säure 2 mol Base.
entspricht 1 mol Säure 2 mol Base.
-
Wie erkenne ich, ob ich über den Endpunkt hinaus titriert habe?Du erkennst Übertitration daran, dass der Indikatorfarbton „zu stark“ und dauerhaft bleibt oder der Messwert (pH, Potential, Leitfähigkeit) deutlich hinter den Sprungbereich weiterläuft. Das passiert, weil dann Überschuss an Maßlösung vorliegt. Deshalb titrierst du nahe am Endpunkt tropfenweise und spülst die Kolbenwand ab.
-
Welche typischen Handhabungsfehler verfälschen das Volumen bei der Bürette am stärksten?Große Fehler entstehen durch Luftblasen in der Bürettenspitze, falsches Ablesen des Meniskus und einen nicht konditionierten Aufbau. Luftblasen machen das abgegebene Volumen scheinbar kleiner, falsches Meniskus-Ablesen verschiebt jeden Messpunkt. Konditioniere Bürette und Pipette, indem du sie mit der jeweiligen Lösung vor dem Start spülst.
Konduktometrie
Um noch mehr über die Konduktometrie zu erfahren, schaue dir unbedingt unser Video und unseren Beitrag dazu an!