Was die Schrödinger Gleichung ist und was sie überhaupt aussagt, genau das erfährst du hier.
Schau dir auf jeden Fall noch das Video zum Artikel an. Darin sind alle wichtigen Informationen für dich audiovisuell aufbereitet.
Inhaltsübersicht
Schrödinger Gleichung einfach erklärt
Die Schrödinger Gleichung ist das Fundament für fast alle praktischen Anwendungen der Quantenmechanik. Sie beschreibt in Form einer partiellen Differenzialgleichung, die Veränderung eines physikalischen, nicht relativistischen Zustandes nach den Regeln der Quantenmechanik.
Dieser physikalische Zustand ist durch eine Wellenfunktion in der Schrödinger Gleichung repräsentiert. Die Wellenfunktion verändert sich mit der Zeit, aufgrund der Anwendung des Hamilton Operators auf diese. Beim Hamilton Operator handelt es sich um den Energie Operator der Quantenmechanik. Mit ihm gibst du Energiemesswerte und die Zeitentwicklung an.
Daher verändert die Wellenfunktion ihre Form in Abhängigkeit von der Zeit. Du beschreibst damit Prozesse wie die Ausbreitung, Streuung und Interferenz von Teilchen . Mit der Schrödinger Gleichung berechnest du die Energieniveaus der physikalischen Zustände.
Schrödinger Gleichung Herleitung
Du kannst die Schrödinger Gleichung nicht aus der klassischen Physik herleiten. Sie ist ein Postulat, das jedoch aus der Hamiltonfunktion eines gegebenen Problems herleitbar ist.
Eine solche Hamiltonfunktion hat die Form:

Hierbei steht  für die Energie,
für die Energie,  für das Potential,
für das Potential,  für den Impuls,
für den Impuls,  für die Masse,
für die Masse,  für den Ort und
für den Ort und  für die Zeit. Daraus leitest du die Schrödinger Gleichung her, indem du diese klassischen Größen durch entsprechende, quantenmechanische Operatoren ersetzt.
für die Zeit. Daraus leitest du die Schrödinger Gleichung her, indem du diese klassischen Größen durch entsprechende, quantenmechanische Operatoren ersetzt.



 ist die imaginäre Einheit
ist die imaginäre Einheit  ,
,  eine partielle Ableitung
(in diesem Fall nach der Zeit) und
eine partielle Ableitung
(in diesem Fall nach der Zeit) und  das reduzierte plancksche Wirkungsquantum
das reduzierte plancksche Wirkungsquantum
 . Zudem brauchst du für den Impulsoperator
. Zudem brauchst du für den Impulsoperator  den sogenannten Nabla-Operator
den sogenannten Nabla-Operator
 . Bei diesem Operator handelt es sich um einen Vektor
, in welchem jedes Element die partielle Ableitung nach einer Raumdimension darstellt
. Bei diesem Operator handelt es sich um einen Vektor
, in welchem jedes Element die partielle Ableitung nach einer Raumdimension darstellt  .
.
Wendest du diese Operatoren nun auf deine Wellenfunktion  an erhältst du die Schrödinger Gleichung.
an erhältst du die Schrödinger Gleichung.

Hier siehst du einen neuen Operator  . Dieser heißt Laplace-Operator
und ergibt sich aus dem Skalarprodukt
. Dieser heißt Laplace-Operator
und ergibt sich aus dem Skalarprodukt
 . Damit handelt es sich bei ihm um einen Vektor, in welchem jedes Element eine partielle, zweite Ableitung nach einer Raumdimension darstellt.
. Damit handelt es sich bei ihm um einen Vektor, in welchem jedes Element eine partielle, zweite Ableitung nach einer Raumdimension darstellt.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Schrödinger Gleichung Schule
In der Schule lernst du wahrscheinlich eine einfachere Form der Schrödinger Gleichung kennen. Diese ist die stationäre, eindimensionale Schrödinger Gleichung. Mit ihr ist es dir möglich einfachere Probleme zu lösen ohne Kenntnisse über Operatoren, komplexe Zahlen, partielle Ableitung und ähnliches zu haben.
Du fängst an, indem du dir die Schrödinger Gleichung aufschreibst:

Du schreibst den Hamilton-Operator  aus und erhältst
aus und erhältst

Jetzt schreibst du den Nabla-Operator aus und löst die Klammern auf

Durch Äquivalenzumformung bringst du alle Terme auf eine Seite

Nun multiplizierst du mit  und klammerst
und klammerst  aus
aus

Zur Vereinfachung wurde hier das Potential  durch die, aus der Schule bekannte Schreibweise für die potentielle Energie
durch die, aus der Schule bekannte Schreibweise für die potentielle Energie
 , ersetzt.
, ersetzt.
Jetzt ersetzt du die zweite Ableitung durch die aus der Schule bekannten Form  und schreibst das reduzierte plancksche Wirkungsquantum aus
und schreibst das reduzierte plancksche Wirkungsquantum aus  .
.
Auf diese Weise erhältst du die Schreibweise wie du sie in vielen Schulbüchern findest

Stationäre Schrödinger Gleichung
Im vorherigen Kapitel hast du bereits den Begriff der stationären Schrödinger Gleichung gelesen. Dabei handelt es sich um einen Spezialfall der Schrödinger Gleichung.

Sie beschreibt Systeme, bei welchen die Funktionswerte  und
und  nur vom Ort, nicht aber von der zeit abhängen. Eine andere Bezeichnung ist auch zeitunabhängig Schrödinger Gleichung.
nur vom Ort, nicht aber von der zeit abhängen. Eine andere Bezeichnung ist auch zeitunabhängig Schrödinger Gleichung.
Schrödinger Gleichung Potentialtopf
Mit der schulphysikalischen Gleichung berechnen wir jetzt ein bekanntes und häufig gesehenes Beispiel, den linearen Potentialtopf.
Die einfache, stationäre Schrödinger Gleichung lautet

Innerhalb des Potentialtopfes mit einer Länge  ist die potentielle Energie Null
ist die potentielle Energie Null  . Die Gesamtenergie entspricht also der kinetischen Energie
und vereinfacht unsere Gleichung somit zu
. Die Gesamtenergie entspricht also der kinetischen Energie
und vereinfacht unsere Gleichung somit zu

Eine bekannte und mögliche Lösungsfunktion ist die Wellenfunktion für stehende Wellen .

Für diese muss die Bedingung für stehende Wellen mit zwei festen Enden gültig sein.
 und
und 
Setzt du das in die Wellenfunktion ein, erhältst du
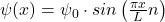
Nun brauchst du noch die zweite Ableitung dieser Funktion. Du erhältst

Formst du jetzt nach  um liefert dir die Gleichung die diskreten Energiewerte des Potentialtopfes.
um liefert dir die Gleichung die diskreten Energiewerte des Potentialtopfes.

Die eingesetzte Wellenfunktion ist also eine Lösung der Schrödinger Gleichung.
Schrödinger Gleichung Wasserstoff
Zuletzt betrachte dir die Schrödinger Gleichung des Wasserstoff Atoms. Im Gegensatz zum linearen Potentialtopf gibt es nun drei Raumdimensionen. Damit hängt die Wellenfunktion 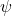 nicht mehr nur noch von
nicht mehr nur noch von  ab, sondern zudem noch von
ab, sondern zudem noch von  und
und  .
.
Zudem bewegt sich das Elektron im elektrischen Potential
des Kerns. Damit ist die potentielle Energie nicht Null, sondern hängt vom Abstand des Elektrons
zum Kern ab.
Damit ergibt sich für die potentielle Energie in Abhängigkeit vom Abstand folgender Zusammenhang

Das ergibt das sogenannte Coulomb-Potential.
Eingesetzt in die Schrödinger Gleichung erhältst du für Wasserstoff

Da die ausführliche Lösung dieses Problems sehr aufwendig ist und den Rahmen dieses Artikels sprengen würde beschränken wir uns hier auf eine Betrachtung der Lösungen.
Das Potential im Wasserstoffatom ist radialsymmetrisch. Somit bietet es sich an die Ortskoordinaten durch Kugelkoordinaten
auszudrücken. Dabei wird ein Punkt durch seinen Abstand vom Ursprung  und zwei Winkel
und zwei Winkel  (Polarwinkel) und
(Polarwinkel) und  (Azimutwinkel) definiert.
(Azimutwinkel) definiert.
Die Koordinaten rechnen sich wie folgt um:



Für den Grundzustand des Wasserstoffatoms erhältst du die Lösungsfunktion

Beachte, dass im Nenner des rechten Exponenten der numerische Wert des Bohr’schen Atomradius auftaucht.
Die sich daraus ergebenen Energieniveaus stimmen mit jenen der Bohr’schen Theorie
überein.

Die Zahl  ist die Hauptquantenzahl
. Sie kann nur Werte positiver, natürlicher Zahlen einnehmen.
ist die Hauptquantenzahl
. Sie kann nur Werte positiver, natürlicher Zahlen einnehmen.
